можно ли лечить суставы антибиотиками
Ревматоидный и инфекционный артрит: в чем отличия от артроза
Боль в суставах и отечность беспокоят людей разных возрастов. Такие симптомы бывают после травм, из-за возрастных изменений или врожденных аномалий, а также вследствие воспалительных процессов. Наиболее распространенные патологии – артроз и артрит. Между ними есть принципиальные отличия.
Боль в суставе и отечность – очень неприятные явления
Ревматоидный артрит: что это и как его лечат
Ревматоидный артрит – это заболевание аутоиммунно-воспалительного характера. Поражает оно чаще женщин разного возраста, при этом страдают суставы лодыжек, коленей, кистей и голеностопы.
Считается, что причина ревматоидного артрита – сбой в работе иммунной системы, а провоцирующие факторы – переохлаждение, стресс, инфекция или травма. Запустить механизм разрушения сустава может грипп, ангина или обычная ОРВИ. Разпознать заболевание достаточно просто:
В отличие от артроза, при котором боль, наоборот, усиливается после физических нагрузок, при ревматоидном артрите разминка сустава помогает избавиться от дискомфорта.
Со временем суставы деформируются и ограничиваются в подвижности. Болезнь охватывает все новые сочленения. В колене скапливается патологическая жидкость – образуется киста Бейкера с риском разрыва. Воспаляется часто и шейный отдел позвоночника – появляются боли в шее и под затылком.
Иногда люди с ревматоидным артритом значительно худеют
Как лечат ревматоидный артрит
На первичной консультации ревматолог назначит дополнительные обследования – анализ крови, рентген сустава, УЗИ или МРТ. Полностью вылечить заболевание невозможно, поэтому терапия направлена на то, чтобы снять неприятную симптоматику и предотвратить осложнения.
При правильном лечении ремиссия длится очень долго, а иногда болезнь полностью отсупает, однако лечиться придется долгие годы. А вот массировать или прогревать суставы, пораженные ревматоидным артритом, категорически нельзя. Подобные манипуляции приводят к обострениям.
При ревматоидном артрите массаж и прогревание противопоказаны
Что такое инфекционный артрит
Причина инфекционного артрита – вирус, грибок или бактерия. Микроорганизмы попадают в суставную полость с током крови или лимфы из другого очага инфекции в организме. Так бывает, например, при открытой травме сустава, после пункции или артротомии – врачебного вмешательства в сустав.
В остром периоде артрит инфекционной природы имеет такие симптомы:
Иногда инфекционный артрит переходит в хроническую форму, и симптомы изменяются:
Инфекционный артрит поражает один крупный сустав
Как лечат инфекционный артрит
Заболевание опасно из-за возможных осложнений, поэтому лечение нужно начать как можно раньше. В зависимости от типа возбудителя пациенту назначают антибиотики, противовирусные или противогрибковые препараты. Также показана симптоматическая терапия – жаропонижающие, обезболивающие и противовоспалительные препараты. В сложных случаях прибегают и к хирургии.
Чем вызван инфекционный артрит и как он проявляется? Рассказывает практикующий врач:
В чем отличия в лечении артритов и артроза
Артроз – не воспалительное, а дегенеративное заболевание суставов, или износ хряща. Заболевание стоит на третьем месте в мире по распространенности после онкологии и сердечно-сосудистых патологий. Симптомы болезни несколько напоминают артрит, но опытный ортопед или ревматолог легко дифференцирует их:
Поскольку острое воспаление, как правило, отсутствует, терапия остеоартроза направлена на борьбу с болью и увеличение подвижности. В схему лечения не включают антибиотики, протиогрибковые или иммуномодулирующие препараты. Ее составляют из таких медикаментов и терапевтических методов:
При артрозе очень важен режим дня
Несмотря на схожую симптоматику, артроз и артрит лечатся совершенно по-разному. Поэтому при появлении суставной боли никогда не стоит заниматься самодиагностикой и тем более самолечением, не нужно испытывать на себе народные способы. С одной стороны, вы рискуете запустить болезнь и довести ее до глубокой хронической стадии. С другой – можете навредить себе и подвергнуть опасности другие органы, например сердце или почки.
Новое в лечении ревматоидного артрита
В последнее время тактика лечения ревматоидного артрита значительно изменилась. Новое в лечении ревматоидного артрита – это отказ от выжидательной позиции и раннее назначение агрессивного курса терапии. Это привело к тому, что специалистами была признана обратимость патологического процесса на ранних стадиях заболевания при назначении активной терапии сразу после установления диагноза.
Врачи клиники «Парамита» используют самые современные методы и лекарственные препараты для помощи больным ревматоидным артритом, сочетая их назначение с методами восточной терапии.
Ревматоидный артрит в цифрах
По современным представлениям ревматоидный артрит (РА) – это сложное многофакторное, хроническое, неуклонно прогрессирующее, системное аутоиммунное заболевание, в основе которого лежит длительный воспалительный процесс в организме с язвенно-деструктивным поражением и разрушением суставов.
Поражение РА населения составляет около 1% всего населения земного шара. Болеют лица любого возраста, от младенцев до пожилых людей, чаще женщины. По статистике ревматоидный артрит был установлен на 1-м году заболевания у 57,9% пациентов, остальные лечились по поводу недифференцированного (неустановленного вида) артрита (НДА), а это значит, не получали необходимой терапии. Еще через год у 33% больных этой группы был выявлен РА, то есть, их лечение замедлилось еще почти на год.
Новейшие принципы лечения РА
В последние десятилетия сформировались основные принципы терапии ревматоидных поражений, их придерживаются специалисты всего мира.
Принцип первый – ранее выявление
Лечить ревматоидные процессы непросто, результат во многом зависит от результатов обследования, установленного диагноза и предполагаемого прогноза болезни. Выявить ревматоидную патологию на ранней стадии сложно, так как похожие симптомы наблюдаются и при других заболеваниях. Поэтому очень большое значение придается выявлению РА и установлению развернутого диагноза, позволяющего сделать прогноз течения болезни у данного больного и назначить ему адекватные лечебные мероприятия.
Диагноз ревматоидного артрита ставится на основании:
ФК (функциональный класс) ревматоидного процесса позволяет оценить сохранность трудовых навыков. По степени их нарушения выделяют 4 ФК.
Диагноз должен включать в себя клиническую и рентгенологическую стадии заболевания, активность патологического процесса, наличие/отсутствие РФ и системных поражений. Это позволит подобрать больному наиболее подходящую схему лечения.
Принцип второй – раннее назначение медикаментозной терапии
Схемы лечения ревматоидного артрита нового поколения учитывают клинически подтвержденный факт, что при раннем назначении активных лечебных мероприятий патологический процесс можно остановить и даже повернуть вспять. Поэтому главной целью является раннее выявление заболевания с назначением адекватного лечения, а непосредственными задачами:
Современная тактика ведения ревматоидных поражений – это агрессивная тактика, когда больному назначается комплексное лечение с максимальными дозировками основных (базисных) противовоспалительных препаратов (БПВП). При этом противовоспалительные средства подбираются по результатам обследования. Раз в квартал проводится текущее обследование с целью проверки результативности проводимой базисной терапии. В состав медикаментозной терапии обязательно вводятся биологические препараты.
Принцип третий – сокращение симптоматической терапии
Новое в лечении ревматоидного артрита – это еще и подход к симптоматической терапии. Сейчас отказались от стандартных схем применения обезболивающих и общих противовоспалительных средств. Их назначают строго индивидуально при наличии воспалительной боли и обязательно сочетают с приемом базисных медицинских препаратов.
Допускается даже нерегулярный прием лекарств из группы нестероидных противовоспалительных препаратов (НПВП) – их принимают по мере необходимости максимально короткими курами или одноразово, используя только один препарат этой группы. Это связано с побочными эффектами НПВП – они вызывают эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ). Еще одна опасность применения этой группы препаратов в том, что на ранних стадиях заболевания они быстро снимают все симптомы заболевания и создают иллюзию полного выздоровления. Это часто приводит к отказу больного от дальнейших лечебных мероприятий и прогрессированию ревматоидного процесса.
Еще одна группа препаратов для лечения ревматоидных поражений – глюкокортикостероиды (ГКС). Они оказывают, как симптоматическое, так (частично) и патогенетическое действие, подавляя процесс разрастания соединительной ткани в суставах, деструкцию хрящевой и костной ткани. На первых начальных стадиях ревматоидного процесса их назначают только при наличии выраженного болевого синдрома воспалительного характера – ГКС отлично снимают воспаление и боль, после чего их отменяют.
Но есть категории больных, в основном это лица преклонного возраста, которым не подходят препараты базисной терапии. В таких случаях эту роль берут на себя ГКС, назначаемые продолжительными курсами в низких дозировках. Иногда их вводят в суставы. Назначение их требует регулярного обследования больного из-за возможных побочек: остеопороза, язвенных процессов в ЖКТ и т.д.
В последние годы препараты этой группы все чаще назначают короткими курсами в высоких дозировках (пульс-терапия). Показаниями для таких процедур лечения являются тяжелые системные поражения (сердца, печени, почек).
Принцип четвертый – двигательная активность
Она необходима для профилактики контрактур и анкилозов (снижение объема движений в суставе или его полная неподвижность), а также мышечных атрофий необходима даже в период обострений – назначается щадящий комплекс лечебной физкультур – ЛФК. По мере улучшения состояния больного нагрузки увеличиваются.
Одновременно назначаются курсы лечебного массажа и физиотерапевтических процедур, усиливающих эффект ЛФК. Для сохранения нормального положения конечности назначают ношение ортезов, но только по нескольку часов в день – постоянное ношение ортезов считается неприемлемым. Двигательная активность значительно улучшает качество жизни больных с ревматоидными поражениями.
Препараты для медикаментозного лечения
Все препараты от ревматоидного артрита делятся на симптоматические и базисные. Симптоматические – это НПВП и ГКС, а базисные – синтетические и биологические.
Лекарственные средства этой группы угнетают образование фермента циклооксигеназы (ЦОГ). ЦОГ делится на два вида: ЦОГ-2, участвующую в синтезе простагландинов, поддерживающих воспаление и боль, и ЦОГ-1, поддерживающую синтез простагландинов, стимулирующих секрецию слизи в органах пищеварения и защищающих стенки органов от различных воздействий.
НПВП, подавляющие только ЦОГ-2 (Нимесулид, Мелоксикам), – это лекарства нового поколения. Они обладают селективным (избирательным) действием и почти не имеют побочного действия на ЖКТ при правильном применении. Они также применяются в современной практике.
Глюкокортикоидные гормоны
Глюкокортикоиды (Преднизолон, Дексаметазон, Метипред) назначаются при тяжелом течении ревматоидных процессов, сильных болях и поражении внутренних органов. В зависимости от состояния пациента эти препараты назначают или достаточно длительно малыми дозами (например, пожилым больным с противопоказаниями для базисной терапии), или короткими курсами очень большими дозами (пульс-терапия). Введение гормональных препаратов в полость сустава может приостановить его воспаление и формирование контрактуры.
Синтетические базисные противовоспалительные препараты
Синтетические базисные препараты применяются достаточно давно, но не потеряли своей актуальности. Курс начинается с назначения одного препарата этой группы. При высокой активности РА лечение начинают с Метатрексата, при средней и небольшой – с Сульфасалазина или Плаквенила. За эффективностью терапии тщательно наблюдают и если эффект есть, но недостаточный, присоединяют еще один базисный препарат (синтетический или биологический). Если эффекта нет, препарат меняют.
Биологические (генно-инженерные) БПВП – биологические агенты
Внутрисуставные инъекции гиалуроновой кислоты
Хондропротекторы что это как выбрать, насколько они эффективны
Инфекционный артрит
Человек постоянно контактирует с окружающей средой, а значит и с населяющими ее микроорганизмами, многие из которых являются патогенными, способными вызвать воспалительный процесс. Инфекционный артрит развивается при попадании инфекции в сустав. Предупредить тяжелые осложнения этого заболевания может только своевременное обращение за медицинской помощью.
Общие сведения о заболевании
Инфекционный артрит – это воспаление сустава, вызванное местной или общей инфекцией. Симптомы болезни и ее течение во многом зависят от вызвавшей инфекционный процесс инфекции.
Коды инфекционных артритов по МКБ-10:
Заболевание очень распространено и может стать причиной стойкого нарушения суставной функции. Четверть пациентов, обращающихся по поводу заболеваний суставов, страдают инфекционными артритами.
Причины инфекционного артрита
Причиной заболевания является инфекция – гнойная инфекция из расположенных рядом очагов (флегмон, абсцессов) или занесенная с током крови при холециститах тонзиллитах, а также общие инфекционные заболевания. При попадании инфекционных возбудителей в сустав иммунная система начинает с ними бороться, вызывая воспалительный процесс, течение которого напрямую связано с особенностями инфекционного возбудителя.
Воспаление может быть:
Инфекционные артриты имеют два механизма развития:
Факторы, предрасполагающие к развитию инфекционного артрита: вредные привычки, поднятие тяжестей, наличие лишней массы тела, сахарного диабета. Гнойные поражения суставов особенно часто развиваются у женщин, страдающих ревматоидным артритом.
Симптомы инфекционного атрита
Инфекционный артрит обычно начинается и протекает остро, иногда подостро. Но при некоторых специфических инфекциях он имеет незаметное начало и длительное течение.
Начало болезни и первые симптомы
При остром начале основными симптомами инфекционного артрита являются: выраженная лихорадка, озноб, летучие мышечно-суставные боли в сочетании с резкой болезненностью в пораженном суставе, отеком и гиперемией кожи над ним. Практически всегда остро протекает инфекционный артрит у детей.
Подострое течение имеет не такое заметное начало, температура тела нормальная или субфебрильная. Отек, гиперемия и боль в суставах умеренные.
Самым опасным является скрытое, незаметное течение, характерное для туберкулезного артрита. Характерны неопределенные боли в суставах, похрустывание, снижение двигательной активности. Болезнь протекает на фоне туберкулеза, небольшое повышение температуры также может не привлечь внимания, поэтому туберкулезный артрит редко выявляется на ранних стадиях.
Явные симптомы
Острый гнойный артрит развиваются очень быстро, состояние ухудшается с каждым днем, беспокоит лихорадка, отечность, гиперемия и боль нарастают. Не исключено, что больному потребуется хирургическая помощь.
При более медленном течении симптомы инфекционного артрита развиваются постепенно, появляется общее недомогание, слабость, суставные боли становятся постоянными, усиливаясь при движении. Постепенно нарушается функция конечностей: появляются трудности в их сгибании или разгибании.
Когда необходимо обращаться за медицинской помощью
К врачу нужно обращаться при появлении следующих симптомов:
Опасности
Заболевание часто протекает тяжело, с осложнениями.
Стадии заболевания
Течение болезни связано с ее клинической формой, поэтому стадии развития патологического процесса могут иметь значительные различия. Рассмотрим стадии развития острого гнойного артрита, разработанные НИИ им. Вишневского:
Возможные осложнения
Инфекционный артрит может давать ранние и поздние осложнения. К ранним осложнениям относятся в основном осложнения гнойного артрита:
Отдаленные последствия – это утрата функции конечности разной степени: от легкой до полной неподвижности.
Классификация
Происхождение и симптомы инфекционного артрита разных клинических форм имеют, как сходство, так и отличие. Рассмотрим наиболее распространенные формы.
Острый гнойный
Данная форма заболевания развивается при попадании в сустав гноеродной инфекции (синегнойной палочки, стафилококков, стрептококков и др.). Заражение может быть первичным при ранениях и вторичным – при переходе инфекции из окружающих тканей или отдаленных очагов инфекции. К группе риска относятся лица, страдающие ревматоидным артритом, особенно, женщины.
Начинается заболевание остро и протекает тяжело. Появляется лихорадка, головная боль, озноб. Пораженный сустав отекает, кожа над ним краснеет. Боль настолько сильная, что больной не может пошевелить конечностью и старается придать ей положение, вызывающее наименьшую болезненность.
Септический
Туберкулезный
Артрит в данном случае также протекает в виде бактериально-метастатической и токсико-аллергической форм. В первом случае поражаются в основном позвоночник и крупные суставы конечностей, а заболевание носит название костно-суставного туберкулеза. Протекает изначально хронически с нарастающими болями при движении, общим недомоганием. Основные изменения видны на рентгене в виде поражения суставной костной ткани от появления пятна с утратой костью кальция до разрушения кости. При отсутствии лечения приводит к инвалидности.
Токсико-аллергическая форма впервые описанная Понсе в начале 20-го века, протекает очень похоже на ревматоидный артрит с хроническим началом и поражением мелких суставов кисти и стоп. Возможна также их деструкция и инвалидизация. Поражение крупных суставов иногда протекает без последствий и проходит на фоне противотуберкулезной терапии.
Хондропротекторы что это как выбрать, насколько они эффективны
Боль в суставах в состоянии покоя
Гонорейный
Поражение суставов гонококковой инфекцией может иметь бактериально-метастатическую и токсико-аллергическую формы. В обоих случаях поражаются крупные суставы, чаще всего один коленный (голеностопный, лучезапястный). Протекает болезнь остро, с высокой температурой, интоксикацией и сильнейшими суставными болями. Колено отекает, краснеет, до него невозможно дотронуться из-за болей.
При проведении своевременного лечения болезнь имеет благоприятный исход. Если же не лечить, быстро наступает полная неподвижность конечности.
Боррелиозный
Боррелиоз или болезнь Лайма – это инфекция, вызываемая спиралевидными бактериями – спирохетами боррелиями. Передается она клещами и протекает в виде последовательной смены стадий:
Вирусный
Развивается на фоне различных вирусных заболеваний:
Грибковый
Чаще всего грибковые поражения суставов развиваются при актиномикозе, но встречаются и при другой грибковой инфекции. Патогенные грибки попадают в суставную полость из расположенного рядом костного очага поражения или из отдаленных очагов (кариозные зубы) с током крови. Течение хроническое, с рецидивами и возможным присоединением бактериальной инфекции. Очень часто возникают свищи – ходы, по которым гной из сустава выделяется на поверхность кожи. При отсутствии адекватного лечения приводит к постепенной утрате суставной функции.
Паразитарный
Причиной артрита обычно является эхинококкоз, поражающий костную ткань позвонков, костей таза и длинных костей конечностей. В суставах обычно развивается токсико-аллергический воспалительный процесс. Часто вовлекаются суставы позвоночника, тазобедренные, коленные и локтевые суставы. Течение доброкачественное, но сопровождается сильными суставными болями. Выздоровление наступает при назначении полноценного лечения эхинококкоза.
Инфекционно-аллергический артрит
Инфекционно-аллергический артрит возникает, когда есть аллергия, на фоне которой развивается при неблагоприятных условиях воспалительный процесс в суставах. Заболевание протекает в бурной форме, сопровождается высокой температурой и сильными болевыми признаками. В области поражения наблюдается покраснение, отечность, припухлость. На разных участках кожи – кольцеобразная аллергическая сыпь. Лечением инфекционно-аллергического артрита занимаются ревматолог и аллерголог.
Локализация инфекционного артрита
При инфекционном поражении суставов локализация патологического процесса зависит от особенностей инфекции и ее клинической формы. При острых гнойных артритах – это в основном крупные суставы – коленный, голеностопный, локтевой. Мелкие суставы кисти и стопы поражаются при токсико-аллергической форме туберкулезного и некоторых вирусных артритах.
Асимметричное поражение одного-двух крупных суставов характерно для боррелиоза, чаще всего при этой инфекции в процесс вовлекаются коленные суставы.
Рациональное применение антибиотиков в ревматологии: избранные аспекты
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В современных условиях борьба с инфекциями и инфекционными осложнениями представляет собой одну из наиболее актуальных проблем медицины. При этом важное место отводится рациональной терапии антиинфекционными препаратами. В ревматологии необходимость применения антибиотиков связана по меньшей мере с двумя факторами: эрадикацией возбудителя-триггера (инфекционного агента, запускающего иммунопатологические механизмы воспаления), а также лечением коморбидной инфекции.
Несмотря на обширный арсенал антимикробных средств, разработанных и внедренных в клиническую практику в течение последних 60 лет, вопросы рациональной терапии инфекционной патологии в различных областях медицины, в т. ч. в ревматологии, по-прежнему требуют к себе самого пристального внимания как в научном, так и в практическом плане.
А-стрептококковый тонзиллит/фарингит
В настоящее время доказана тесная ассоциация острой ревматической лихорадки (ОРЛ) с высоковирулентными («ревматогенными») А-стрептококковыми штаммами, компоненты которых обусловливают иммунизирующий эффект и развитие иммуноопосредованного патологического процесса. Имеющиеся на сегодняшний день данные свидетельствуют о том, что по крайней мере в пределах нескольких следующих десятилетий человечество не сможет быть избавлено от β-гемолитического стрептококка группы А (БГСА). Таким образом, сохраняется возможность вспышек ОРЛ в различных регионах мира, особенно среди детей в возрасте 7–15 лет.
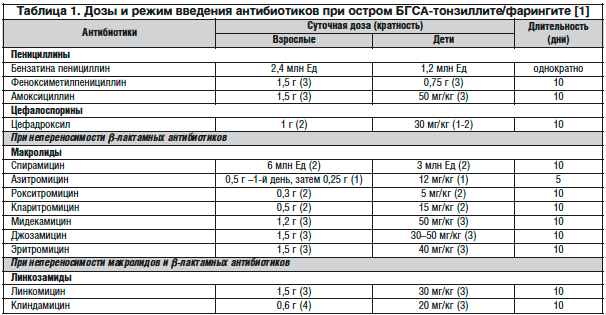
В соответствии с современными рекомендациями пенициллин V (феноксиметилпенициллин) или амоксициллин рассматриваются в качестве средств выбора для лечения БГСА-инфекции глотки у больных с хорошей переносимостью этих лекарственных препаратов (табл. 1). Оптимальным препаратом из группы оральных пенициллинов является амоксициллин, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но существенно превосходит их по своим фармакокинетическим характеристикам, отличаясь большей биодоступностью (95, 40 и 50% соответственно) и меньшей степенью связывания с сывороточными белками (17, 22 и 60% соответственно).
Назначение ампициллина в пероральной форме для лечения БГСА-тонзиллита, а также инфекций дыхательных путей иной локализации в настоящее время большинством авторов признано нецелесообразным по причине неудовлетворительных фармакокинетических характеристик препарата (в первую очередь – низкой биодоступности).
Применение феноксиметилпенициллина оправданно только у младшего контингента больных, учитывая наличие лекарственной формы в виде суспензии, а также несколько большую комплаентность, контролируемую со стороны родителей, чего нельзя сказать о подростках.
Показаниями к назначению однократной инъекции бензатин пенициллина являются следующие:
При непереносимости β-лактамных антибиотиков целесообразно назначение макролидов (спирамицин, азитромицин, рокситромицин, кларитромицин, мидекамицин, джозамицин), противострептококковая активность которых сопоставима с таковой пенициллина. Эти препараты также обладают способностью создавать высокую тканевую концентрацию в очаге инфекции и хорошей переносимостью. Применение эритромицина – первого представителя антибиотиков данного класса в настоящее время существенно снизилось, особенно в терапевтической практике, поскольку он наиболее часто по сравнению с другими макролидами вызывает нежелательные эффекты со стороны ЖКТ, обусловленные его стимулирующим действием на моторику желудка и кишечника.
В современной действительности приобретенная устойчивость БГСА к эритромицину распространена достаточно широко, и в отдельных европейских регионах она превышает 40%. По данным многоцентрового проспективного исследования ПЕГАС-3, в России за период 2006–2009 гг. резистентность БГСА к макролидам была следующей: эритромицин – 0,8%, кларитромицин – 3,3%, азитромицин – 10%, спирамицин – 1,4%, джозамицин – 1,7%, мидекамицин – 4,1% [2].
Общепризнанно, что в условиях повсеместно нарастающей резистентности БГСА к макролидам эти антибиотики следует рассматривать лишь как альтернативные средства для лечения БГСА-тонзиллита и назначать их только больным с аллергией на β-лактамы. Несоблюдение данного требования, т. е. широкое применение макролидов в качестве стартовой эмпирической терапии БГСА-инфекции глотки, может повлечь за собой весьма серьезные последствия вплоть до развития ОРЛ [3].
Длительность лечения БГСА-инфекции глотки макролидами составляет 10 дней, азитромицином – 5 дней. Согласно последним данным [4, 5], ранее одобренная Фармкомитетом РФ схема (10 мг/кг/сут в 1 прием в течение 3-х дней, курсовая доза – 30 мг/кг) значительно уступает по бактериологической эффективности как 5-дневной схеме (12 мг/кг/сут в 1 прием в течение 5 дней, курсовая доза – 60 мг/кг), так и препаратам сравнения.
Антибиотики-линкозамиды (линкомицин, клиндамицин) также обладают высокой противострептококковой активностью, но их назначают при БГСА-тонзиллите только при непереносимости β-лактамов и макролидов. Широкое применение этих препаратов при данной нозологической форме не рекомендуется. Известно, что при частом применении оральных пенициллинов чувствительность к ним со стороны зеленящих стрептококков, локализующихся в ротовой полости, существенно снижается. Поэтому у данной категории пациентов, среди которых достаточное количество больных с ревматическими пороками сердца и клапанными протезами, линкозамиды рассматриваются как препараты первого ряда для профилактики инфекционного эндокардита при выполнении различных стоматологических манипуляций.
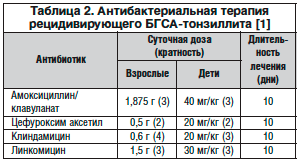
При наличии хронического рецидивирующего БГСА-тонзиллита достаточно высока вероятность колонизации очага инфекции микроорганизмами, продуцирующими специфические ферменты – β-лактамазы, которые обусловливают гидролиз пенициллиновых антибиотиков. В этих случаях целесообразно проведение курса лечения ингибитор-защищенными пенициллинами (амоксициллин/клавуланат) или оральными цефалоспоринами II поколения (цефуроксим аксетил), а при непереносимости β-лактамных антибиотиков – линкозамидами (табл. 2). Указанные антибиотики также рассматриваются как препараты второго ряда для случаев безуспешной пенициллинотерапии острого БГСА-тонзиллита (что чаще встречается при использовании феноксиметилпенициллина). Универсальной схемы, обеспечивающей 100% элиминацию БГСА из носоглотки, в мировой клинической практике не имеется.
Необходимо отметить, что применение тетрациклинов, сульфаниламидов, ко-тримоксазола и хлорамфеникола при БГСА-инфекции глотки в настоящее время не оправданно по причине высокой частоты резистентности и, следовательно, низких показателях эффективности терапии. Назначение ранних фторхинолонов (ципрофлоксацин, пефлоксацин, офлоксацин, ломефлоксацин) также не обоснованно по причине низкой природной противострептококковой активности этих препаратов. Фторхинолоны II поколения – так называемые «респираторные» (левофлоксацин, моксифлоксацин), несмотря на их высокую противострептококковую активность, не показаны для стандартного лечения БГСА-инфекций глотки из-за широкого спектра антимикробного действия (что может послужить побудительным моментом к формированию резистентности к этим препаратам со стороны других возбудителей инфекций), менее благоприятного (по сравнению с пенициллином) профиля нежелательных лекарственных реакций, а также более высокой стоимости.
Реактивные артриты
Реактивные артриты (РеА) – это воспалительные негнойные заболевания суставов, развивающиеся в тесной хронологической связи (обычно не позднее чем через 2 мес.) с перенесенной кишечной или урогенитальной инфекцией. Согласно заключению международной экспертной комиссии [6], определенными триггерами постэнтероколитических или энтерогенных РеА (ЭРеА) признаны иерсинии, шигеллы, сальмонеллы и кампилобактер, урогенных РеА (УРеА) – Chlamydia trachomatis. В качестве возможных триггеров УРеА рассматриваются уреаплазмы и гонококки. РеА относятся к группе серонегативных спондилоартритов и, как правило (около 80%), ассоциируются с наличием антигена HLA-B 27.
На сегодняшний день большинством авторов признано целесообразным раннее назначение антибиотиков при остром РеА, ассоциированном с хламидийной инфекцией. Следует отметить, что санация организма больного УРеА от хламидийной инфекции представляет собой достаточно сложную задачу. Показано, что при УРеА практически у всех больных воспалительный процесс в урогенитальном тракте не ограничивается уретрой, а распространяется на вышележащие отделы его, что значительно затрудняет санацию этого очага. Данное обстоятельство в определенной степени может служить объяснением того, что 7–10-дневные курсы антибиотикотерапии, применяемые для лечения неосложненного урогенитального хламидиоза, совершенно не эффективны при РеА, ассоциированном с хламидийной инфекцией. Однако даже при адекватной длительной антимикробной терапии частота бактериологических неудач при РеА может достигать 40%, что, по всей видимости, связано с биологическими особенностями возбудителя.
Известно, что носители видовых признаков хламидий – элементарные тельца – метаболически не активны, существуют во внеклеточной среде и в ряде случаев могут неопределенно долгое время находиться в состоянии покоя. Более того, у пациентов с РеА, которые ранее уже лечились антибиотиками, возможно развитие персистирующей инфекции, когда изначально метаболически активные ретикулярные тельца, локализующиеся внутри клетки, останавливаются на определенном этапе развития и не превращаются в элементарные тельца. Эти промежуточные формы по сравнению с обычными имеют меньшие размеры и не чувствительны к действию антибиотиков.
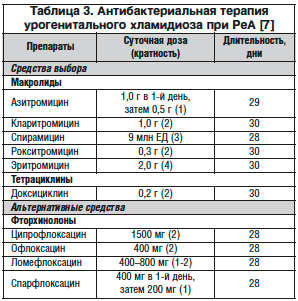
Для лечения урогенитального хламидиоза при РеА в качестве препаратов выбора рекомендуются антибиотики из групп макролидов или тетрациклинов (табл. 3), назначаемые в течение 28–30 дней. При непереносимости или неэффективности указанных препаратов применяют фторхинолоны.
Контрольные исследования на хламидиоз следует выполнять через 1, 2 и 3 мес. после окончания лечения. Контроль излеченности предпочтительно проводить методом выделения хламидий в культуре клеток. В случае невозможности проведения данного исследования рекомендуется использование 2-х методов диагностики хламидийной инфекции: иммунофлуоресцентного и метода полимеразной цепной реакции (ПЦР). Использование серологических методов диагностики не рекомендуется, т. к. хламидийные антитела обнаруживаются не у всех больных текущим хламидиозом, а IgG-антитела могут сохраняться в крови достаточно долго после излечения от инфекции.
Как свидетельствует опыт, накопленный в НИИР РАМН, частота эрадикации Chlamydia trachomatis у больных РеА колеблется от 65 до 76%, что является весьма действенным стимулом к постоянному поиску новых схем и методов лечения данной инфекции у этих пациентов.
В целом, признавая необходимость длительного применения антибиотиков при РеА, ассоциированном с хламидийной инфекцией, следует отметить, что единого мнения в отношении схем лечения в мировой литературе нет. Для решения этой проблемы необходимы широкомасштабные многоцентровые клинические исследования. Вопрос о влиянии антибиотиков на поражение суставов при УРеА остается дискуссионным и требует дальнейшего изучения. Однако лечение хламидиоза является необходимым, т. к. эта инфекция относится к заболеваниям, передающимся половым путем. Необходимо также адекватное лечение половых партнеров этих лиц. В то же время общепризнанно, что назначение антибиотиков при ЭРеА является нерациональным, поскольку к моменту развития суставного синдрома возбудитель в большинстве случаев уже элиминируется из макроорганизма.
Боррелиоз Лайма (иксодовые клещевые боррелиозы)
В последние годы ревматологи проявляют неослабевающий интерес к боррелиозу Лайма (БЛ), поскольку при этой инфекции нередко встречается поражение опорно-двигательного аппарата. Клинические проявления обусловлены наличием живого микроба в тканях, поэтому для купирования симптомов необходимо достаточно длительное антибактериальное воздействие. Возбудители БЛ чувствительны к широкому спектру антибактериальных препаратов (тетрациклины, пенициллины, цефалоспорины II–III генераций, макролиды) и в то же время устойчивы к аминогликозидам, фторхинолонам, сульфаниламидам. Вследствие неэффективности (или отсутствия доказательств эффективности) не рекомендуются к применению для любой стадии БЛ цефалоспорины I генерации, карбапенемы, ванкомицин, метронидазол, изониазид, рифампицин. Антибактериальные препараты назначаются как перорально, так и парентерально в разовых и курсовых дозах в зависимости от выраженности клинических проявлений и периода болезни. Доказано, что ранняя (т. е. назначенная по поводу клещевой мигрирующей эритемы) антибактериальная терапия снижает риск развития вторичной эритемы и поражения суставов и, таким образом, является важным фактором дальнейшего благоприятного течения БЛ. Выявлена высокая степень корреляции между лечением, начатым в первый месяц болезни, и выздоровлением. Таким образом, при БЛ прогноз четко коррелирует не только с оптимальной антибактериальной терапией, но и с ранними сроками ее начала. Применительно к ревматологии это означает, что своевременная адекватная терапия локальной кожной инфекции, по сути, является первичной профилактикой развития артрита и других системных осложнений. В таблице 4 представлены схемы антибактериальной терапии БЛ, разработанные экспертами Американского общества инфекционных болезней. Необходимо отметить, что лечение антибиотиками является обязательным во всех случаях БЛ независимо от давности и стадии заболевания.
При Лайм-артрите без сопутствующих неврологических симптомов лечение начинают с доксициклина. Преимущества такого подхода – пероральный прием, меньшая частота побочных действий и более низкая стоимость препарата. При одновременном развитии Лайм-артрита и неврологических проявлений рекомендуют цефтриаксон. Альтернативные антибиотики – цефотаксим или пенициллин G. Повторный курс проводится не ранее чем через 3 мес., т. к. эффект антимикробной терапии наступает медленно. При персистенции или рецидивах артрита рекомендуется 4-недельный курс лечения пероральными препаратами или цефтриаксоном в течение 2–4 нед. Повторное лечение антимикробными средствами, начатое поздно, может быть малоэффективным. При его неэффективности добавляются нестероидные противовоспалительные препараты, глюкокортикоиды внутрисуставно, проводится артроскопическая синовэктомия.
Для лечения пациентов детского возраста на ранней стадии рекомендуется амоксициллин или цефуроксима аксетил. При поражении нервной системы и хроническом Лайм-артрите оптимальным является цефтриаксон. В качестве альтернативы возможно использование цефотаксима. Продолжительность лечения – 2–4 нед.
На фоне лечения антибиотиками примерно у 5–10% больных (обычно при использовании пенициллина или цефалоспоринов) может развиться реакция Яриша–Герксгеймера. Она возникает, как правило, в 1-е сут от начала лечения при остром и на 2–3 сут при хроническом вариантах течения болезни. Основные проявления реакции: озноб, повышение температуры, головные и мышечные боли, усиление местных кожных реакций в области очагов эритемы (увеличение ее размеров, отечности и болезненности), лейкоцитоз, а также ухудшение общего самочувствия больного. Важно отличать эту реакцию от аллергической реакции на антибиотик. Реакция Яриша–Герксгеймера не рассматривается в качестве основания для отмены применяемого антибиотика, т. к. она не является результатом непереносимости препарата больными и обычно быстро купируется либо самостоятельно, либо в результате усиления дезинтоксикационной терапии.
При БЛ микробиологические критерии излеченности для практики недоступны. По этой причине исследования, посвященные изучению связи между чувствительностью микроорганизма к данному антибиотику in vitro и клиническим исходом, не проводились. Применяемые схемы лечения носят рекомендательный характер, их эффективность основывается только на клиническом опыте. На практике результаты лечения оценивают по динамике клинических симптомов. Эффективность терапии на ранней стадии БЛ оценивают через 6–12 мес., поскольку поздние проявления болезни могут развиться в течение года после лечения мигрирующей эритемы.
По окончании курса антибактериальной терапии у ряда больных сохраняются плохое самочувствие, головные боли, снижение памяти, нарушение концентрации внимания, неопределенные мышечно-скелетные боли, признаки хронической усталости, вегетативной дисфункции и др. Эти симптомы, объединяемые термином «постлаймский» синдром, персистируют от 6 до 18 мес. и значительно снижают качество жизни пациента, перенесшего болезнь Лайма. Доказано, что назначение антибактериальной терапии больным с постлаймским синдромом к улучшению не приводит.
Только для зарегистрированных пользователей






