можно ли пить бисептол с метронидазолом
Подходы к лечению больных синдромом избыточного бактериального роста в тонкой кишке, развившимся в связи с патологией верхних отделов желудочно-кишечн
В статье оценивается эффективность терапии синдрома избыточного бактериального роста (СИБР) в тонкой кишке у больных с патологией верхних отделов желудочно-кишечного тракта (ЖКТ). В исследование включено 30 больных с патологией верхних отделов ЖКТ с СИБР.
In this paper, we assess efficiency of therapy of excessive bacterial growth syndrome in small intestine in patients with pathology of upper segments of gastrointestinal tract (GIT). The study included 30 patients with pathology of upper segments of GIT and excessive bacterial growth syndrome (EBGS). The main reasons of EBGS development in the studied patients were chronic pancreatitis with pancreas exocrine insufficiency and conducting eradication therapy in patients with duodenal ulcer associated with Н. pylori.
Синдром избыточного бактериального роста (СИБР) определяется как состояние, при котором повышено содержание микробов в тонкой кишке. У здоровых людей количество бактерий в тощей кишке составляет 10 3–4 КОЕ/мл, увеличиваясь до 10 7 /мл в подвздошной кишке. Количественной границей, позволяющей констатировать СИБР, является выявление ≥ 10 5 колониеобразующих единиц/мл (КОЕ/мл) в аспирате из проксимальных отделов тонкой кишки [1].
Факторами, препятствующими колонизации тонкой кишки микробами из вышележащих отделов, являются: соляная кислота, пепсин, желчные кислоты, лизоцим, секрет поджелудочной железы, нормальная моторика кишечной трубки, функционирующий илеоцекальный клапан, секреторный иммуноглобулин А. Повреждения этих защитных механизмов (снижение секреции соляной кислоты, панкреатической и билиарной секреции, применение антибиотиков, нарушение моторики кишечника, несостоятельность илеоцекального клапана, нарушение продукции секреторных иммуноглобулинов и др.) приводят к развитию СИБР, появлению разнообразной клинической симптоматики (расстройство стула, метеоризм, абдоминальные боли и др.) и возникновению мальдигестии и мальабсорбции [1].
Для диагностики СИБР могут быть использованы инвазивные и неинвазивные методы. При использовании инвазивных методов проводят аспирацию содержимого двенадцатиперстной или проксимальных отделов тонкой кишки или забор биоптата с последующей культивацией аспирата или биоптата. Методики имеют определенные ограничения: невозможность культивации 20–60% микробов в лабораторных условиях, контаминация проб во время их забора, высокий процент ложноотрицательных результатов, низкая воспроизводимость и др. [2, 3]. К непрямым методам относятся тесты, основанные на изучении метаболитов микрофлоры после нагрузки тем или иным субстратом (лактулозой, глюкозой, лактозой и др.). Лактулоза является искусственным синтетическим дисахаридом, состоящим из фруктозы и галактозы, который не переваривается пищеварительными ферментами человека, но ферментируется водородпродуцирующими бактериями желудочно-кишечного тракта. В норме лактулоза разлагается и утилизируется бактериями в толстом кишечнике с образованием водорода, который всасывается в кровь и выделяется с выдыхаемым воздухом. При СИБР лактулоза подвергается брожению в тонкой кишке, вследствие чего концентрация водорода возрастает раньше, чем в норме [4].
Тактика ведения больных предполагает выявление и воздействие на причину развития СИБР, а на сам СИБР, при его устойчивом характере, путем проведения антибактериальной терапии. Возможно использование разных антибактериальных препаратов: метронидазола, тетрациклина, Бисептола, ципрофлоксацина, ванкомицина, рифаксимина. Выбор антибактериального препарата зависит от путей миграции микробной флоры. Так как при изучаемой патологии флора поступает из дыхательных путей и верхних отделов желудочно-кишечного тракта, для проведения настоящего исследования был избран Бисептол.
Бисептол — комбинированный противомикробный препарат, состоящий из сульфаметоксазола и триметоприма. Сульфаметоксазол, сходный по строению с парааминобензойной кислотой (ПАБК), нарушает синтез дигидрофолиевой кислоты в бактериальных клетках, препятствуя включению ПАБК в ее молекулу. Триметоприм усиливает действие сульфаметоксазола, нарушая восстановление дигидрофолиевой кислоты в тетрагидрофолиевую — активную форму фолиевой кислоты, ответственную за белковый обмен и деление микробной клетки. Препарат обладает широким спектром противомикробной активности, включающим большинство грамотрицательных (Salmonella spp. (включая Salmonella typhi и Salmonella paratyphi), Escherichia coli (энтеротоксигенные штаммы), Proteus spp., Klebsiella spp., Entеrobacter spp., Shigella spp., Yersinia spp.) и грамположительных (Streptococcus spp., Staphylococcus spp., Enterococcus faecalis, Streptococcus pneumoniae, Bacillus anthracis, Listeria spp., Nocardia asteroides) аэробных бактерий.
В исследовании проводилась оценка эффективности препарата Бисептол (сульфаметоксазол 400 мг, триметоприм 80 мг) в коррекции синдрома избыточного бактериального роста у больных с патологией верхних отделов желудочно-кишечного тракта.
Задачами исследования были:
1) оценка клинической эффективности на основании анализа дневника пациента и динамики клинических данных;
2) изучение динамики результатов водородного теста;
3) определение динамики результатов карболеновой пробы;
4) исследование переносимости и безопасности терапии по частоте развития клинических побочных эффектов, динамике клинического и биохимического анализов крови.
1) наличие СИБР по данным водородного дыхательного теста;
2) больные язвенной болезнью, ассоциированной с инфекцией Н. pylopi, хроническим атрофическим гастритом со сниженной секреторной функцией;
3) больные, длительно получающие ИПП;
4) больные после проведения антибактериальной терапии (эрадикация и др.);
5) больные хроническим панкреатитом с внешнесекреторной недостаточностью поджелудочной железы;
6) больные с хронической патологией печени и желчевыделительной системы и сниженной продукцией желчи.
Материал и методы исследования
Изучено 30 больных с патологией верхних отделов желудочно-кишечного тракта с синдромом избыточного бактериального роста, отвечающих критериям включения.
Дизайн исследования
На первом визите проводили оценку состояния больного, сбор анамнеза и необходимые диагностические процедуры: водородный тест, оценка времени транзита карболена по пищеварительному тракту — карболеновая проба, клинический анализ крови, биохимический анализ крови (АЛТ, АСТ, билирубин, ЩФ, ГГТ, мочевина, креатинин). При соответствии пациента критериям включения назначали препарат Бисептол по 2 таблетки 2 раза в день в течение 7 дней. Оценку клинических симптомов проводили в баллах по следующим градациям: 0 — нет, 1 — симптом выражен слабо, 2 — симптом выражен умеренно, 3 — симптом выражен сильно, 4 — симптом выражен очень сильно и требует лечебной коррекции. На втором визите (на 8-й день) проводили осмотр пациента, оценивали физикальные данные и клинические проявления в баллах. Проводили контрольные исследования (водородный тест, карболеновую пробу, клинический анализ крови, биохимический анализ крови (АЛТ, АСТ, билирубин, ЩФ, ГГТ, мочевина, креатинин)). Оценивали переносимость и безопасность по клиническим (нежелательные явления) и лабораторным данным.
Результаты исследования
В исследование были включены 30 больных: 14 женщин, 16 мужчин. Средний возраст составил 52,3 ± 16,8 года. Заболевания, которые привели к развитию СИБР, представлены в табл. 1.
Основными причинами развития СИБР у исследуемых больных были: хронический панкреатит (ХП) с внешнесекреторной недостаточностью поджелудочной железы (ВСНПЖ) и проведение эрадикационной терапии у больных язвенной болезнью двенадцатиперстной кишки (ЯБДК), ассоциированной с Н. pylori. Из 13 больных ХП с ВСНПЖ, у 8 по данным эластазного теста фиксировалась умеренная ВСНПЖ (эластаза I кала от 100 до 200 мкг/г), у 5 пациентов — тяжелая (менее 100 мкг/г). У всех пациентов проводилась адекватная заместительная ферментная терапия микронизированными препаратами (Креон, Эрмиталь) в суточных дозах 100 000–150 000 Ед липазной активности в зависимости от исходной степени ВСНПЖ.
У 14 больных язвенной болезнью (12 пациентов с локализацией язвы в двенадцатиперстной кишке, 2 — сочетанной локализации) проводилась эрадикационная терапия в течение 10 дней. У 7 пациентов проводилась последовательная терапия (Омитокс 20 мг 2 раза в день + амоксициллин 1000 мг 2 раза в день 5 дней, затем Азитрал 500 мг 2 раза в день — 5 дней). У 7 больных — тройная терапия первой линии (Омез 20 мг 2 раза + амоксициллин 1000 мг 2 раза + кларитромицин 500 мг 2 раза). Другие возможные причины развития СИБР включали нарушенную моторику кишечника у больной с синдромом раздраженного кишечника (диарея) и билиарную недостаточность у больных с патологией печени с нарушением желчевыделения (жировой гепатоз и дисфункция желчного пузыря, холестероз желчного пузыря).
Оценка клинической эффективности
Клинические проявления СИБР оценивали в баллах по данным индивидуального дневника. Их динамика после 7-дневного курса терапии представлена в табл. 2. Основным симптомом у изучаемых пациентов был метеоризм, который беспокоил практически всех пациентов. Другие жалобы (переливание, учащенный кашицеобразный стул, боли по ходу кишки, урчание) наблюдали с частотой 46,7–76,7%. После проведенного курса терапии достоверно уменьшилась интенсивность представленных симптомов, увеличилось количество пациентов с оформленным стулом.
Результаты изучения водородного теста до и после лечения
Водородный дыхательный тест с нагрузкой лактулозой проводили с использованием анализатора Gastrolyzer. Измеряли базальный уровень концентрации водорода в выдыхаемом воздухе, который не должен превышать 10 ppm (в этом случае от проведения водородного дыхательного теста воздерживались как минимум на 16 часов из-за возможного получения ложных результатов). Далее пациенту давали 10 г лактулозы. После первого (натощак) измерения уровня водорода последующий замер производили через 15 мин, затем на 15-й, 30-й, 45-й, 60-й, 90-й и 120-й минутах.
СИБР констатировали при повышении концентрации водорода более чем на 10 ppm от базального уровня в течение от 15 до 60 мин. Как правило, максимальное повышение концентрации водорода фиксируется не ранее 60-й минуты теста, чаще после 90-й минуты, поскольку именно столько времени требуется для прохождения лактулозы в толстую кишку. При увеличении концентрации водорода раньше этого времени возможны два варианта СИБР.
Первый вариант: СИБР с полноценной функцией илеоцекального клапана.
При исследовании выявляется кривая с двумя пиками. Появление первого пика повышения концентрации водорода свидетельствует о наличии СИБР в тонкой кишке с полноценной функцией илеоцекального клапана и о том, что бактерии, находящиеся в тонкой кишке, способны метаболизировать лактулозу. Второй пик свидетельствует о том, что большая часть лактулозы не абсорбируется в тонкой кишке и подвергается процессу ферментации в толстой кишке.
Второй вариант: СИБР сочетается с нарушением функции илеоцекального клапана. При этом варианте кривая характеризуется быстрым повышением концентрации водорода (в течение 60 мин), которое сохраняется до 90-й минуты, превышая исходный уровень как минимум на 20 ррm и отсутствием снижения ее между первым и вторым наивысшим показателем. В таких случаях можно предполагать ретроградный заброс химуса из толстой кишки в тонкую кишку (терминальную часть подвздошной кишки) через илеоцекальный клапан, что приводит к СИБР в терминальном отделе тонкой кишки.
До лечения первый вариант СИБР наблюдали у 10 (33,3%), второй вариант — у 20 (66,7%) пациентов. Исчезновение СИБР после проведенного курса лечения отметили у 20 (66,7%) больных. При этом эффективность лечения зависела от исходного варианта СИБР: из 10 больных с первым вариантом (с полноценной функцией илеоцекального клапана) разрешение СИБР по данным водородного теста наступило у 8 (80%); при втором варианте эффект лечения наблюдали у 12 (60%) из 20 пациентов. Основная патология также влияла на эффективность терапии СИБР. Из 14 больных язвенной болезнью коррекция СИБР наступила у 12 (85,7%). При ХП положительный результат лечения наблюдали у 7 (53,8%) из 13 пациентов. В связи с малым размером выборки представленные различия и в том, и в другом случае не достоверны.
Результаты изучения карболеновой пробы до и после лечения
Карболеновая проба использовалась для оценки времени кишечного транзита и состояла в назначении пациенту 4 таблеток активированного угля с фиксацией времени визуального определения появления угля в кале и оценки времени пассажа карболена по кишечнику. До лечения средние значения времени кишечного транзита составляли 12,5 ± 4,8 часа, после лечения продолжительность увеличилась до 14,4 ± 3,4 часа (р ≤ 0,05, различия достоверны).
Оценка переносимости и безопасности проводимой терапии
Переносимость и безопасность проводимой терапии оценивали по частоте развития (нежелательных явлений) побочных эффектов, динамике клинического и биохимического анализов крови.
Нежелательные явления наблюдали у двух больных. У одной больной возникла горечь во рту, которая была выражена умеренно, купировалось самопроизвольно, отмена Бисептола не проводилась. У одного пациента развилась крапивница, которая купировалось при приеме Супрастина. Отмена препарата не проводилась. Таким образом, частота нежелательных явлений составила 6,7%. Выраженность их можно расценить как слабую, связь с приемом изучаемого препарата как вероятную.
Какой-либо динамики основных показателей клинического и биохимического анализов крови после лечения не наблюдали.
Обсуждение
Эффективность терапии была выше у больных СИБР с сохраненной функцией илеоцекального клапана — 80% — по сравнению с вариантом с несостоятельностью илеоцекального клапана, где она составила 60%. Это можно объяснить тем, что при первом варианте СИБР основной микрофлорой, попадающей в тонкую кишку из вышележащих отделов желудочно-кишечного тракта, полости рта, верхних дыхательных путей, являются аэробы. Бисептол обладает широким спектром противомикробной активности, включающим грамотрицательную и грамположительную аэробную микрофлору. При втором варианте (попадание микробов из толстой кишки при нарушенной функции илеоцекального клапана) существенная роль принадлежит контаминации тонкой кишки анаэробной микрофлорой из толстой, на которую Бисептол не действует. Таким образом, данные водородного теста позволяют более обоснованно осуществлять выбор антибактериальной терапии СИБР: при сохраненной функции илеоцекального клапана и преобладающем заселении тонкой кишки микрофлорой из верхних отделов желудочно-кишечного тракта возможно назначение Бисептола, при нарушении функции илеоцекального клапана есть основания для выбора препарата, воздействующего на анаэробную микрофлору, контаминирующуюся из толстой кишки.
Коррекция СИБР по результатам водородного теста сопровождалась положительной динамикой клинической картины с исчезновением или существенным снижением выраженности симптомов. Сохранение измененных результатов водородного теста, как правило, сочеталось с отсутствием положительной динамики симптомов.
Результаты настоящего исследования показали, что эффективность Бисептола в лечении СИБР у больных с патологией верхних отделов желудочно-кишечного тракта составила 66,7%. Терапия приводила к достоверному снижению интенсивности симптомов, характеризующих СИБР, а также увеличению времени кишечного транзита. Переносимость и безопасность препарата была хорошей, частота побочных эффектов составила 6,7%, интенсивность их была слабой. Изменений в показателях клинического и биохимического анализов крови не наблюдали.
Выводы
Литература
ФГБУ ДПО ЦГМА УД Президента РФ, Москва
Лечение обострений хронических заболеваний органов пищеварения
Создание ряда высокоэффективных фармакопрепаратов обеспечило существенное повышение эффективности лечения больных с патологий органов системы пищеварения. Среди этих лекарственных средств заслуживают внимание блокаторы Н2-рецепторов гистамина (ранитидин,
П. Я. Григорьев, доктор медицинских наук, профессор
Э. П. Яковенко, доктор медицинских наук, профессор
А. П. Яковенко, кандидат медицинских наук
Н. А. Агафонова, А. С. Прянишников, П. В. Гуляев, Е. В. Таланова, С. Б. Кальнова
Создание ряда высокоэффективных фармакопрепаратов обеспечило существенное повышение эффективности лечения больных с патологий органов системы пищеварения. Среди этих лекарственных средств заслуживают внимание блокаторы Н2-рецепторов гистамина (ранитидин, фамотидин и др.), ингибиторы протонной помпы (омепразол, лансопразол, пантопразол, рабипразол), прокинетики (цизаприд, домперидон, прукелоприд и др.), полиферментные препараты (креон, панцитрат, мезим-форте, ликреаза и др.), противовирусные (интерфероны, рибавирин, ламивудин и др.), а также антибактериальные и противопаразитарные средства. При оптимальном их использовании быстро и надежно достигается ремиссия гастроэзофагеальной рефлюксной болезни, язвенной болезни желудка и двенадцатиперстной кишки, предупреждается развитие осложнений язвенной болезни и геморрагического гастродуоденита. Нередко удается ингибировать репликацию вирусов, купировать активность и прогрессирование хронических вирусных гепатитов В и С и предупредить трансформацию хронического гепатита в цирроз и цирроз-рак печени.
В настоящее время в патогенезе острого и хронического гастрита, дуоденита, язвенной болезни желудка (ЯБЖ), язвенной болезни двенадцатиперстной кишки (ЯБДПК), MALT-лимфомы желудка и даже рака желудка доказана роль Helicobacter pylori (Нр). Обсуждается роль Нр-инфекции в патогенезе ряда экстрагастральных заболеваний: ишемической болезни сердца, мигрени, цирроза печени и др.
Разработка и внедрение в практику комбинированной антигеликобактерной лекарственной терапии ЯБЖ и ЯБДПК радикально изменили прогноз этих и некоторых других заболеваний желудка и двенадцатиперстной кишки.
Оптимальными вариантами эрадикационной терапии при ЯБЖ, ЯБДПК и эрозивных гастритах (гастродуоденитах), ассоциированных с Нр, признаны семидневные трех- или четырехкомпонентные схемы. Трехкомпонентная схема включает омепразол 20 мг, или лансопразол 30 мг, или пантопразол 40 мг, или пилорид (ранитидин висмут цитрат) 400 мг, которые принимаются с интервалом в 12 часов + кларитромицин 250 мг 2 раза в день или амоксициллин 500 мг 4 раза в день или 1000 мг 2 раза в день, или тетрациклин 500 мг 4 раза в день или 1000 мг 2 раза в день + метронидазол 400 мг 2 раза в день или фуразолидон 0,2 г 2 раза в день. Четырехкомпонентная 7-10-дневная эрадикационная терапия используется, если предыдущий вариант оказался неэффективным, и включает омепразол 20 мг 2 раза в день, или лансопразол 30 мг 2 раза в день, или пантопразол 40 мг 2 раза в день + препараты висмута (вентрисол или де-нол 120 мг 4 раза в день или бисмофальк 2 табл. 3 раза в день) + тетрациклина гидрохлорид 500 мг 4 раза в день, или амоксициллин 500 мг 4 раза в день + метронидазол 250 мг 4 раза в день или фуразолидон 0,1 г 4 раза в день. При этом все антибактериальные препараты необходимо принимать во время еды. В четырехкомпонентной схеме целесообразно использовать комбинированный препарат гастростат, в состав которого входят эти же ингредиенты. Другие комбинации использовать не рекомендуется в силу их малой эффективности.
После окончания 7-10-дневной эрадикационной терапии необходимо продолжить лечение при ЯБЖ в течение семи недель, при ЯБДПК — пяти недель, при эрозивном гастродуодените — трех недель одним из следующих антисекреторных препаратов: ранитидин 300 мг в сутки, фамотидин 40 мг в сутки, омепразол 20 мг в сутки, лансопразол 30 мг в сутки, пантопразол 40 мг в сутки. В качестве симптоматических средств дополнительно могут использоваться антациды (маалокс и др.) и цитопротекторы (вентер и др.).
Вышеуказанная терапия более чем в 90% случаев приводит к эрадикации Нр. В результате этого купируется активное воспаление в слизистой оболочке (СО) желудка и двенадцатиперстной кишки, обеспечивается заживление эрозий и язв, предупреждается развитие обострений и осложнений (кровотечение, прободение, стенозирование), лимфомы и, возможно, рака желудка.
Отечественные ученые обращают внимание практических врачей на то, что нередко имеет место гипердиагностика язвенной болезни и гастрита (гастродуоденита), не раскрываются причины возникновения болезней, не учитывается, что эрозивно-язвенный процесс в гастродуоденальной СО носит гетерогенный характер и не всегда связан с ЯБ. Так, например, при остром гастрите также могут появляться эрозии, локальные участки кровоизлияний в СО и кровотечения. При гистологическом исследовании у таких больных в СО выявляются умеренные признаки воспаления. Наиболее частыми причинами такого острого гастрита (гастродуоденита) являются: химические повреждения СО (алкоголь, нестероидные противовоспалительные средства, агрессивные щелочные жидкости), вирусы (цитомегаловирус, вирусы герпеса), бактерии (гемолитические стрептококки и др.), уремия, радиационные облучения. Изредка некоторые микробы вызывают даже острый флегмонозный гастрит. Ученым удалось установить причины стрессового гастрита, факторами риска развития которого являются: гипоксия, заболевания печени и почек, тяжелые операции, ожоги, сепсис, травмы ЦНС. Нередко в течение 24 часов после воздействия стрессовых факторов в СОЖ возникают острые эрозии и язвы. При этом приблизительно у 30% больных наблюдаются желудочно-кишечные кровотечения, причем у части из них они бывают массивными, угрожающими жизни. У пострадавших с ожогами часто диагностируются повреждения СО верхних отделов пищеварительного тракта, которые получили название «язвы Курлинга», при которых, особенно локализующихся в ДПК, существует большой риск не только развития кровотечений, но и перфораций. У больных с травмой головы и инсультом нередко в гастродуоденальной СО обнаруживаются острые язвы (язвы Кушинга). При этих язвах, особенно дуоденальной локализации, также существует большой риск развития кровотечений и перфораций. Поэтому необычайно важно выделять людей с высоким риском возникновения стрессовых повреждений ЖКТ и как можно раньше начинать лечение антисекреторными препаратами для профилактики развития кровотечения и перфорации.
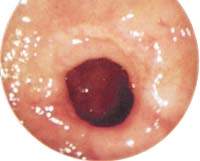 |
| Поверхностная язва привратника |
Отечественными учеными проведено немало исследований с целью установления связи между приемом нестероидных противовоспалительных средств (НПВС) и повреждениями ЖКТ. У больных, принимающих данные препараты по поводу ревматоидного артрита, остеоартроза и других болезней, язвообразование отмечается в 15-20% случаев, часто возникают осложнения (кровотечения и перфорации), особенно у лиц, имеющих в анамнезе ЯБ. Суммарный риск поражения ЖКТ у принимающих НПВС приблизительно в три раза выше, чем у не принимающих эти препараты. У пожилых пациентов (старше 65 лет) такой риск возрастает в пять раз. Врачи, назначающие данные препараты, обязаны предусмотреть решение трех задач: предупреждение развития НПВС-индуцированных язв (особенно при наличии факторов риска), их лечение (часто в условиях, когда требуется продолжение приема НПВС), а также профилактика повреждений СО тонкой и толстой кишки, возникающих при длительном их приеме. Несмотря на то что в лечебную практику начинает внедряться новый класс НПВС (селективные ингибиторы циклооксигеназы-2), которые не должны оказывать повреждающего эффекта на СО ЖКТ, их безопасность требует клинического подтверждения, и данные исследования к настоящему времени еще не завершены.
Главная задача профилактики стрессового гастрита и в известной мере НПВС-ассоциированных повреждений гастродуоденальной СО — увеличение рН внутрижелудочного содержимого до 4 и выше, так как при данном уровне рН происходит инактивация протеолитического фермента пепсина и повышение коагуляции крови. На сегодняшний день с этой целью целесообразно воспользоваться блокаторами Н2-рецепторов гистамина (ранитидин, фамотидин и др.) или ингибиторами протонной помпы (омепразол, лансопразол, пантопразол).
Отечественные и зарубежные ученые большое внимание уделили также изучению различных форм хронического гастрита (ХГ). Наряду с ХГ, связанным с Нр, и ХГ типа А, выделяются эозинофильный, лимфоцитарный и гранулематозный (болезнь Крона, туберкулез, гистоплазмоз, сифилис, саркоидоз и др.) гастриты, а также гипертрофические гастропатии (болезнь Менетрие, псевдолимфома желудка, синдром Золлингера — Эллисона), застойная гастропатия при портальной гипертензии (не является истинным гастритом), щелочной (желчный) рефлюкс-гастрит. При некоторых формах ХГ развивается гипо- и ахлоргидрия и недостаточность витамина В12. По мнению отечественных ученых, клиническая значимость ХГ состоит в том, что он может считаться ранним предраковым заболеванием, развитие которого происходит от атрофии СО к кишечной метаплазии и далее к раку желудка. Диагноз ХГ должен всегда основываться только на результатах квалифицированного гистологического исследования прицельно взятых биоптатов СОЖ, на что имеются указания в упомянутых выше государственных стандартах.
Одним из наиболее распространенных кислотозависимых заболеваний является гастроэзофагеальная рефлюксная болезнь (ГЭРБ), для лечения которой разработаны рекомендации и определены обязанности больного и врача.
Больному рекомендуется: спать на кровати с приподнятым не менее чем на 15 см головным концом; снизить массу тела, если имеется патологическое ожирение; не ложиться после еды в течение 1,5 часа; не принимать пищу перед сном, ограничить прием жира; прекратить курить и употреблять алкоголь; избегать тесной одежды, тугих поясов, а также работы в наклонном положении тела; по возможности ограничить прием лекарственных средств, оказывающих отрицательное влияние на моторику пищевода и тонус нижнего пищеводного сфинктера (пролонгированные нитраты, антагонисты кальция, теофиллин, миогенные спазмолитики, а также препараты, повреждающие СО пищевода (аспирин и другие аналоги).
Медикаментозное лечение назначается дифференцированно в зависимости от выраженности клинических, функциональных и морфологических изменений в верхних отделах пищеварительного тракта. При гастроэзофагеальном рефлюксе без эзофагита (есть симптомы, но нет видимых изменений СО пищевода) используются два варианта терапии. В случаях если ГЭРБ сочетается с замедлением эвакуации из желудка, снижением тонуса нижнего пищеводного сфинктера, гипомоторной дискинезией кишечника, целесообразно назначать внутрь прокинетики — мотилиум (домперидон) 10 мг или координакс (цизаприд, перистил и другие аналоги) 5-10 мг 4 раза в день в сочетании с буферными антацидами (маалокс или аналоги) по одной дозе через час после еды и одну дозу непосредственно перед сном. После достижения клинической ремиссии продолжается «терапия по требованию», то есть прерывистое симптоматическое лечение (при изжоге — мотилиум + антацид или быстрорастворимый зантак — 150 мг). При наличии выраженной недостаточности нижнего пищеводного сфинктера и/или высокого уровня интрагастральной кислотности целесообразно использовать блокаторы Н2-рецепторов гистамина (ранитидин 150 мг 2 раза в сутки или фамотидин 20 мг 2 раза в сутки), а при их неэффективности — ингибиторы протонной помпы (омепразол 20 мг в сутки или ланзопразол 30 мг в сутки) до достижения клинической ремиссии. В дальнейшем назначается «терапия по требованию», предусматривающая при появлении симптомов ГЭРБ прием антисекреторных препаратов в половинной суточной дозе или антацидов.
При рефлюкс-эзофагите I степени в течение 6 недель используются блокаторы Н2-рецепторов гистамина — ранитидин 150 мг, или фамотидин 20 мг 2 раза в день с интервалом в 12 часов, или ингибиторы протонной помпы — омепразол 20 мг в сутки или ланзопразол 30 мг в сутки. При наступлении ремиссии (в среднем через 6 недель) больного переводят на терапию «по требованию» с использованием антацидов, или Н2-блокаторов, или ингибиторов протонной помпы.
При рефлюкс-эзофагите III-1V степени на 4 недели назначается ингибитор протонной помпы омепразол 20 мг или лансопразол 30 мг 2 раза в день с интервалом в 12 часов. Далее, при купировании симптомов ГЭРБ продолжается прием омепразола 20 мг в сутки или лансопразола 30 мг в сутки до 8 недель с последующим переходом на постоянную поддерживающую терапию с использованием вышеуказанных препаратов в половинной суточной дозе в течение года. При недостаточной эффективности данной терапии возможно сочетание антисекреторных средств с прокинетиками-мотилиумом или координаксом в обычных суточных дозах. К дополнительным средствам терапии рефрактерных форм ГЭРБ относят сукральфат (вентер, сукрат-гель) 1,0 г 4 раза в день за 30 минут до еды в течение одного месяца.
Практический врач часто встречает больных с синдромом избыточного бактериального роста (СИБР) и изменением состава микрофлоры в кишечнике, называемым дисбактериозом. К возникновению этого синдрома могут приводить разные причины: болезни органов пищеварения, сопровождающиеся секреторно — моторными нарушениями, особенно при наличии очагов воспаления; перенесенные острые кишечные инфекции (бактериальная дизентерия, иерсиниозный энтероколит и др.); длительный прием лекарственных средств, влияющих на секрецию пищеварительных желез, регенерацию эпителия и моторно-эвакуаторную функцию пищеварительного тракта; длительный, а иногда и нерациональный прием антибактериальных препаратов; неполноценное питание; алкоголизм. Клинические проявления синдрома избыточного бактериального роста в кишечнике связаны с гиперизбыточной продукцией органических кислот и преждевременной деконъюгацией желчных кислот, выделением бактериальных токсинов, разрушением пищеварительных ферментов, развитием моторных расстройств.
Для СИБР характерно наличие абдоминальных болей или дискомфорта в животе, нарушение стула (изменение формы и нарушение пассажа), вздутие и чувство распирания живота, потеря массы тела, слабость, повышенная утомляемость, раздражительность. Лечение СИБР наряду с соответствующей диетой включает один-два семидневных курса антибактериальной терапии, назначение ферментных препаратов, лекарственных средств, регулирующих моторно-эвакуаторную функцию кишечника и интракишечный уровень рН, устраняющих дефицит витаминов, минеральных элементов и др., то есть проводится комбинированное лечение. Показаниями для назначения антибактериальной терапии являются: 1) избыточный бактериальный рост в тонкой кишке; 2) наличие воспалительных изменений в слизистой оболочке кишечника; 3) выявление условнопатогенной микрофлоры в посевах кишечного содержимого.
При СИБР в тонкой кишке в основном используется один из следующих антибактериальных препаратов: тетрациклина гидрохлорид 250 мг 4 раза в сутки, ципрофлоксацин 250 мг 2 раза в сутки, бисептол 960 мг 2 раза в сутки, метронидазол 500 мг 2 раза в сутки, фуразолидон 100 мг 3-4 раза в сутки, эрсефурил 200 мг 4 раза в сутки, интетрикс 1 капс. 4 раза в сутки, цефалексин 250 мг 4 раза в сутки. В ряде случаев можно применить энтерол 2-4 капсулы или пакета в сутки. При СИБР в толстой кишке предпочтение отдается одному из нижеперечисленных препаратов: фталазол или сульгин 1,0 г в сутки, эрсефурил 800 мг в сутки, интетрикс 4 капсулы в сутки, метронидазол 1,0 г в сутки, бактисубтил 4-6 капсул в сутки.
После окончания курса антибактериальной терапии назначаются пробиотики — препараты, содержащие нормальные штаммы кишечной флоры и пребиотики — средства, обеспечивающие их рост и функциональную активность. Для восстановления микрофлоры тонкой кишки используются пробиотики, содержащие аэробные штаммы (бифиформ 2-4 капсулы в сутки или лактобактерин 5-10 доз в сутки), толстой кишки — пробиотики, включающие анаэробные штаммы (бифидумбактерин 5-10 доз в сутки или колибактерин 5-10 доз в сутки,), толстой и тонкой кишки — комбинированные препараты (бифиформ 2-4 капсулы в сутки или бификол 5-10 доз в сутки). Продолжительность их приема составляет 2-4 недели.
Бифиформ — пробиотик, одна капсула которого содержит бифидумбактерин и энтерококки в объеме не менее 10 в седьмой степени каждого вида бактерий. Капсулы препарата покрыты энтеросолюбильной оболочкой, благодаря чему бактерии доходят до кишечника в неизмененном виде. Наличие в препарате анаэробной флоры делает его универсальным для восстановления микробиоценоза тонкой и толстой кишки. Кроме того, каждая капсула содержит особую питательную среду, необходимую для роста и размножения молочнокислых бактерий, что позволяет выживать и быть метаболически активной микрофлоре, содержащейся в препарате бифиформ.
В проведенном нами исследовании участвовали 119 больных, из них 68 женщин и 51 мужчина в возрасте от 21 до 76 лет (средний возраст 39,7 лет).
Для разработки эффективных подходов к назначению бифиформа нами апробированы три схемы терапии. Первая схема, при которой бифиформ назначался без предшествующей терапии, направленной на деконтаминацию кишечника, была использована у 37 больных. Вторая схема, предусматривающая прием бифиформа после предшествующей деконтаминации кишечника, назначалась 28 больным. Третью схему, при которой лечение бифиформом проводилось в виде монотерапии, получали 24 больных. Больные контрольной группы получали терапию, аналогичную второй схеме, но они не получали бифиформ или другие пробиотики.
Бифиформ назначался по 1 капсуле два раза в день в течение 15 дней. Однако если к седьмому дню лечения тяжесть клинических проявлений уменьшалась менее чем на одну степень, дозу препарата увеличивали до 2 капсул два раза в день и терапия продолжалась еще две недели. Для деконтаминации кишечника и снятия воспалительных явлений у больных с хроническими заболеваниями органов пищеварения проводились от одного до трех курсов противомикробной терапии продолжительностью от пяти до семи дней со сменой препаратов в очередном курсе.
Прием бифиформа оказал положительный эффект на состав кишечной микрофлоры. К концу лечения у 35 (76,1%) больных отмечено восстановление нормальной кишечной микрофлоры, и лишь у 11 (23,9%) состав ее оставался измененным. У большинства больных нормализовалось общее количество кишечной флоры, отмечено увеличение количества кишечной палочки, бифидобактерий, нормализация содержания энтерококков и исчезновение условно-патогенных энтеробактерий (лактозонегативных, гемолизирующих штаммов кишечной флоры, представителей родов Klebsiella, Enterobacter, Proteus, Pseudomonas, Citrobacter и др.). Следует отметить, что у значительной части больных, у которых оставались изменения в составе кишечной флоры, имели место и клинические симптомы (боли в животе, метеоризм, нарушения стула), что подтверждает их патогенетическую связь.
Бифиформ как в комплексном лечении, так и в виде монотерапии показал свою эффективность в купировании клинических проявлений диспепсии, в нормализации процессов пищеварения и восстановлении нормального состава кишечной флоры при широком спектре заболеваний органов пищеварения. Доза бифиформа по 1-2 капсулы два раза в день в течение двух недель является достаточно эффективной в ведении больных с хроническими заболеваниями органов пищеварения.
Отсутствие эффекта от проводимого лечения может быть связано с диетическими нарушениями, психоэмоциональными расстройствами, употреблением алкоголя, но чаще — неполным восстановлением нормальной кишечной микрофлоры в результате неадекватной терапии лекарственными средствами. Успех лечения в известной степени зависит не только от лекарственной терапии, предписываемой врачом, но и от пациента, которому необходимо избавиться от вредных привычек, изменить стиль жизни, пунктуально принимать лекарства и т. д.
Все материалы, поступающие в редакцию, рецензируются независимыми рецензентами и при необходимости редактируются. Редакция не несет ответственности за пропажу рукописи.
Направление в редакцию работ, ранее опубликованных или представленных для публикации в другие издания, не допускается.
Не забывайте указать точный почтовый адрес и телефон для контакта.
.gif)
.gif)
.gif)