можно ли по виду опухоли при узи определить характер роста инвазивный неинвазивный
Можно ли по виду опухоли при узи определить характер роста инвазивный неинвазивный
Тревожные звоночки: гинеколог назвала неочевидные симптомы рака шейки матки
Самые распространенные злокачественные образования — рак шейки матки, рак тела матки и рак яичника. Любой онкологический процесс как в гинекологии, так и в общей практике, зачастую сложно распознать из-за отсутствия ярко выраженных хронических симптомов.
Рак шейки матки — наиболее часто встречающееся заболевание в репродуктивном возрасте, то есть возрасте 35-45 лет.
«Сложность диагностики заключается в том, что рак вызывает симптомы уже на распространенных стадиях, а на начальных стадиях, особенно на первой, устанавливается только на основании гистологического исследования — биопсии — и, по сути, никаких симптомов не вызывает», — прокомментировала доктор.
Наиболее частый симптом, на который врач рекомендует обязательно обращать внимание — это кровянистые выделения из половых путей. Однако практически любой женщине легко запутаться, потому что в этом возрасте у них еще есть регулярные ежемесячные потери крови — это менструация, а потому женщины редко обращают внимание на этот симптом. В таком случае, советует гинеколог, стоит присмотреться к дополнительным признакам рака шейки матки.
Что вас должно насторожить:
«Обозначенные боли в области таза — клинические симптомы того, что онкологический процесс может существовать и может захватывать ближайшую клетчатку и, соответственно, проходящие там нервы и сосуды», — объяснила онколог Ольга Смирнова.
Рак тела матки — это наиболее часто выявляемый диагноз у женщин в возрасте менопаузы, обычно его ставят после 60 лет.
«Здесь тоже основным симптомом являются кровянистые выделения с половых путей. Но, на счастье женщины, в этот период у нее уже никаких кровянистых выделений не бывает, поэтому женщины достаточно быстро обращаются к врачу и наиболее часто болезнь диагностируется на первой стадии заболевания», — рассказала врач-онколог.
В этом возрасте обязательным показанием для обращения к врачу считаются любые кровянистые выделения после того, как у вас полностью закончилась менструация: это уже не норма, поясняет специалист, добавив, что женщину насторожить также должны тянущие боли внизу живота.
Рак яичников является наиболее сложным в диагностике. Данный онкологический процесс возникает в яичниках чаще всего после 45 лет.
«Из-за отсутствия классических симптомов диагностировать рак яичников на ранних стадиях практически невозможно. Обнаруживают его в результате ультразвуковой диагностики, также постановка диагноза может стать случайной находкой после удаления кисты яичника», — призналась научный сотрудник исследовательского центра онкологии.
К слову, такой диагноз, как рак яичников, чаще всего выявляется на распространенных стадиях — второй и третьей.
Тревожными симптомами, по которым можно косвенно определить, что у вас рак яичников, являются:
Зачастую пациенты, находящиеся в группе риска заболеваний яичников, в первую очередь обращаются именно к гастроэнтерологу. Если вдруг вы заметили у себя подобные жалобы, есть основания для того, чтобы незамедлительно показаться доктору и провести необходимые исследования для уточнения диагноза, подытожила гинеколог-онколог Ольга Смирнова.
Что такое НИПТ и почему об этом исследовании столько говорят в последнее время? Какие преимущества у данных тестов? Кому они показаны и существуют ли ограничения? Сегодня мы найдём ответы на эти и другие актуальные вопросы.
Биохимические скрининговые программы не обладают высокой точностью, они основаны на cовокупности данных статистики, уровня гормонов и размеров плода по УЗИ. Амниоцентез – самый точный метод, но он инвазивный (нужно сделать прокол плодного пузыря, чтобы получить для исследования клетки, принадлежащие плоду) и угрожает развитием осложнений и прерыванием беременности.
Медицинская наука не прекращала поиски новых тестов для скрининга, которые были бы более точны и не зависели от расчётных показателей. В качестве скрининговых тестов в последнее время хорошо себя зарекомендовали НИПТ (неинвазивные пренатальные тесты) как надёжные, удобные и не мешающие нормальному протеканию беременности. Точность метода достигает 99,9%, так как исследуется генетический материал плода (его ДНК) в венозной крови будущей матери.
Как это возможно? Учёные выяснили, что начиная примерно с 10 недели беременности в крови женщины свободно циркулирует ДНК плода. Благодаря современным технологиям врачи научились выделять её и исследовать, выявляя самые распространенные изменения хромосом.
Таким образом, почти каждая женщина может сдать венозную кровь, дождавшись срока 10 недель беременности, и определить генетическое здоровье будущего малыша.
В каких случаях исследование с применением НИПТ будет наиболее полезно?
В спектре лаборатории KDL представлено несколько комплексов НИПТ. Они отличаются объёмом исследования, показаниями и ограничениями. Важно чтобы понять, какой тест подходит именно Вам.
В каких случаях выполнение НИПТ невозможно?
Итак, выполнение неинвазивных пренатальных тестов возможно при одноплодной и двуплодной беременности. Если беременность одноплодная естественная или наступила после ЭКО с использованием собственной яйцеклетки, то доступны все исследования НИПТ. В остальных случаях существуют ограничения.
В чем отличия разных тестов линейки НИПТ?
НИПС Т21 (Геномед)- диагностика только синдрома Дауна. В исследовании выявляется дополнительная 21 хромосома, если она есть у плода. Синдром Дауна считается одной из самых частых хромосомных аномалий и его частота растёт с увеличением возраста женщины. Выполняется при беременности вследствие естественного зачатия, при ЭКО с собственной яйцеклеткой или при использовании донорской яйцеклетки; при беременности одним плодом и двойней, а также при суррогатном материнстве и если произошла редукция одного эмбриона в двойне.
НИПС 5 – ДНК тест на 5 синдромов (Геномед) – неинвазивный тест на 5 синдромов, можно определить аномалии 13, 18, 21 и в большинстве исследований выявить аномалии половых хромосом X и Y.
НИПС 5 универсальный, его выполнение возможно как при одноплодной естественной беременности, так и при беременности двойней, при носительстве донорской яйцеклетки, суррогатным матерям и в том случае, когда один плод в двойне редуцирован.
3 тестовые базовые панели:
Базовые панели позволяют выявить хромосомные аномалии 13,18, 21, Х и Y хромосом плода, а также триплоидии.
НИПС (Геномед) – включает определение вышеперечисленных синдромов (скрининг 13, 18, 21, Х, Y хромосом плода) и определение носительства у матери частых мутаций, которые могут привести к наследственным болезням, если ребенок унаследует два дефектных рецессивных гена от обоих родителей или один доминантный ген. Данные мутации выявляются в крови без выделения ДНК плода, т.е. оценивается не хромосомная мутация плода, а наличие аномальных вариантов генов у матери.
Генетические заболевания, связанные в тестируемыми в этом исследовании вариантами генов:
НИПС уникален не только клинической значимостью, но и доступностью. Одноплодная беременность, беременность двойней (с определением зиготности), в том числе при редукции одного из эмбрионов в двойне. При ЭКО с донорской яйцеклеткой и суррогатном материнстве этот тест нецелесообразен, так как определять мутации, связанные с генетическими заболеваниями нужно по крови той женщины, чья яйцеклетка дала начало эмбриону.
Следующие 2 панели включают микроделеционные синдромы:
Микроделеции – это поломки сегмента хромосом, которые являются менее распространенными, но не менее опасными, и их невозможно заподозрить на УЗИ.
НИПТ Panorama, расширенная панель (Natera) – исследуются и стандартные аномалии хромосом (13,18,21, Х, Y, триплоидии) и микроделеционные синдромы. Если у Вас беременность одноплодная естественная или в результате ЭКО с собственной яйцеклеткой, то выполнение данных панелей возможно.
При наличии двух плодов, ЭКО с донорской яйцеклеткой и суррогатном материнстве определить сегментарные нарушения технически невозможно.
Можно ли определить пол плода и в каких случаях?
Да, по желанию женщины любой НИПТ определяет пол плода и это доступно как при одноплодной, так и при двуплодной беременности.
Обращаем Ваше внимание, что получение результатов, указывающих на риски развития патологических синдромов, требует консультации генетика и дополнительной инвазивной диагностики.
Возможности современных ультразвуковых методик в диагностике рака эндометрия
Журнал «SonoAce Ultrasound»
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Согласно мировой статистике, рак тела матки занимает 7-е место среди злокачественных заболеваний. Анализ онкологической ситуации в последнее десятилетие в России свидетельствует о неуклонном росте заболеваемости раком эндометрия, который к 2007 г. занял 2-е место среди всех злокачественных опухолей у женщин. Доля рака тела матки в структуре заболеваемости злокачественными новообразованиями на 100 000 женского населения России в разных регионах колеблется от 4,5 до 22,5. Прослеживается неуклонное возрастание частоты заболеваемости с 9,8 в 1990 г. до 13,9 в 2005 г., что соответствует 3-му месту по величине показателей прироста заболеваемости злокачественными новообразованиями [1]. В настоящее время увеличение числа впервые выявленных случаев рака тела матки не уступает таковому при опухолях молочной железы. В странах третьего мира риск развития рака тела матки в целом ниже, при этом уровень смертности остается высоким. В странах Северной Америки и Европы данное заболевание встречается значительно чаще, являясь наиболее распространенной злокачественной опухолью женской половой системы, и занимает 4-е место среди всех злокачественных новообразований после рака молочной железы, легких и толстой кишки. Заболеваемость раком эндометрия в возрасте от 40 до 54 лет резко повышается, пик заболеваемости приходится на возраст 60-64 года. Частота распространения рака эндометрия и ее динамика в разных странах с учетом влияния миграционных процессов и возраста указывают на специфические особенности заболевания и зависимость его возникновения от комплекса причин эндо- и экзогенной природы [2].
В патогенезе заболевания ведущее значение имеет теория избыточной эстрогенной стимуляции эндометрия, сочетающейся с недостаточностью прогестерона. Как полагают, избыточное влияние эстрогенов может приводить к гиперплазии эндометрия, которая способна прогрессировать в атипический вариант и в 20-25% случаев к переходу в аденокарциному. В то же время существующая зависимость между степенью пролиферации эндометрия и концентрацией эстрогенов в крови отмечается до определенного, порогового значения и даже интенсивная пролиферация не во всех случаях сопровождается злокачественной трансформацией эндометрия. Обнаруженная корреляция между содержанием эстрогенов и повреждением ДНК в нормальном и малигнизированном эндометрии заставляет обращать больше внимания на роль молекулярногенетических и морфологических факторов при формировании разных типов рака тела матки. Рак эндометрия характеризуется гетерогенной природой, что проявляется на уровне как факторов риска, так и его патогенеза, чем определяются особенности формирования групп риска при данном заболевании.
В настоящее время для выявления патологии эндометрия в основном используются диагностическое выскабливание полости матки, гистероскопия и аспирационноцитологическое исследование, а также методы лучевой диагностики, среди которых ведущее значение имеет ультразвуковое исследование (УЗИ) 4. При этом отсутствуют единые методически обоснованные эхографические критерии инвазивного роста опухоли. Внедрение в программы интегрированного обследования больных новых ультразвуковых технологий, таких как импульсная допплерометрия, ультразвуковая ангиография и трехмерная реконструкция изображений, позволило существенно повысить эффективность первичной диагностики и мониторинга больных раком эндометрия в процессе специфической терапии [7, 8].
Целью настоящей работы было изучение возможностей комплексного УЗИ с применением цветового допплеровского и энергетического картирования (ЦДК и ЭК), импульсной допплерометрии и трехмерной реконструкции изображений в первичной и уточняющей диагностике рака эндометрия.
Материал и методы
Особое внимание уделяли оценке глубины миометральной инвазии, возможному переходу злокачественного процесса на цервикальный канал и состоянию регионарных лимфатических узлов, что имело решающее значение при определении стадии заболевания и выборе тактики лечения [12].
Результаты и обсуждение
В результате проведенного исследования у 34 пациенток выявлены гиперпластические процессы эндометрия, которые были выделены нами в отдельные нозологические формы, соответствующие рекомендациям ВОЗ. В табл. 1 представлено распределение больных в зависимости от морфогенеза выявленных гиперпластических процессов эндометрия.
| Количество больных | ||
|---|---|---|
| абс. | % | |
| Морфологическая форма гиперпластических процессов эндометрия | 34 | 100 |
| Железисто-кистозная гиперплазия | 19 | 56 |
| Железисто-фиброзные полипы | 5 | 15 |
| Атипическая гиперплазия | 10 | 29 |
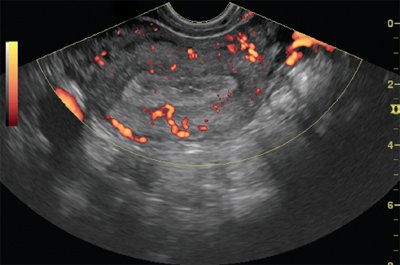
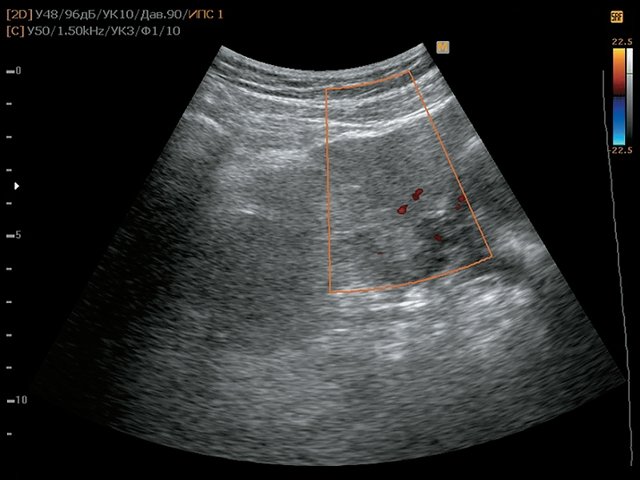
Методикой цветовой допплерографии внутриопухолевый кровоток при железисто-кистозной гиперплазии регистрировался в виде единичных сигналов от сосудов, расположенных по периферии. При фиброзно-железистых полипах визуализировался умеренно выраженный венозный и артериальный периферический кровоток со средними показателями периферического сосудистого сопротивления. У 2 пациенток с железистой гиперплазией определялась выраженная гиперваскуляризация эндометрия. При атипической гиперплазии регистрировался центральный и периферический внутриопухолевый кровоток умеренной интенсивности. У 5 больных с железисто-кистозной гиперплазией при атрофическом эндометрии кровоток не регистрировался. Характерными признаками доброкачественности новообразования даже при наличии множественных полиповидных разрастаний являлись сохранение формы полости матки, четкое определение наружного контура эндометрия и равномерное распределение сосудов миометрия (рис. 1 и 2).
Рис. 1. ТВУЗИ, режим энергетического картирования. Железисто-кистозная гиперплазия эндометрия.
Современная лучевая диагностика, тактика ведения неорганных забрюшинных опухолей
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
Забрюшинное пространство ограничено спереди задним листком брюшины, сзади – позвоночным столбом и мышцами спины, сверху – диафрагмой, снизу – мышцами тазового дна, латерально – мышцами брюшной стенки от уровня передней верхней ости гребня подвздошной кости до переднего конца XII ребра. В этом потенциально большом пространстве опухоли достигают значительных размеров, прежде чем приводят к возникновению каких-либо клинических проявлений, что обусловливает неблагоприятный прогноз злокачественных забрюшинных опухолей.
Неорганные забрюшинные опухоли (НЗО) являются достаточно редкими и встречаются менее чем в 1% случаев среди всех новообразований человека. Данные опухоли относятся к первичным, развивающимся из ретикулярной, жировой и соединительной тканей, фасций, мышц, кровеносных и лимфатических сосудов, лимфатических узлов, расположенных забрюшинно. Метастатические поражения забрюшинных лимфатических узлов, а также образования, органная принадлежность которых определена, не относятся к НЗО [1, 5, 8, 9].
В основном данная группа образований развивается у людей в возрасте от 40 до 60 лет. Наиболее часто встречается среди женщин.
Злокачественный характер образования носят в 60–85% случаев. Одной из особенностей данных опухолей является склонность к рецидивированию, которая, в свою очередь, может достигать 55%, при этом метастазирование имеет место лишь в 33% случаев. Наиболее часто НЗО метастазируют в легкие, печень, значительно реже – в лимфатические узлы, яичники [1, 2, 16].
Случаи малигнизации доброкачественного образования составляют, по данным литературы, менее 1% случаев.
Этиология забрюшинных опухолей мало изучена. К факторам, предрасполагающим к развитию данной группы новообразований, относят воздействие ионизирующего излучения, подтверждением чего служат случаи развития опухолей у пациентов, которым проводилась лучевая терапия по поводу других заболеваний.
В последние десятилетия опубликованы работы, связывающие возникновение сарком, в частности забрюшинного пространства, с использованием в сельском хозяйстве пестицидов и гербицидов.
Классификация
В клинической практике применяются несколько морфологических классификаций НЗО, но чаще всего используется классификация американского врача Лорена Акермана, предложенная в 1954 г. Данная классификация до сих пор сохраняет свою актуальность.
Забрюшинные неорганные новообразования представляют собой гетерогенную группу опухолей, которые подразделяют в зависимости от микроскопических признаков, степени дифференцировки тканей и биологического потенциала.
В целом гистогенетически забрюшинные опухоли можно разделить на три основные группы (внутри которых различают доброкачественные и злокачественные):
Из симпатической нервной системы могут развиваться ганглионевромы, симпатикобластомы или нейробластомы.
Основную массу забрюшинных опухолей составляют первые две группы. Наиболее часто встречаются липосаркома (41%), лейомиосаркома (28%), злокачественная фиброзная гистиоцитома (7%), фибросаркома (6%) [6, 14].
Гистологическая верификация
Клиническое течение забрюшинных опухолей характеризуется большим разнообразием и зависит не только от гистологического строения, но и от степени дифференцировки клеток. Параметрами, определяющими степень дифференцировки новообразования, являются клеточное строение, плеоморфизм клеток, митотическая активность, наличие некрозов и характер роста (экспансивный или инвазивный). Наибольшее значение имеют количество митозов и распространенность некрозов. В соответствии с одной из классификаций принято различать I степень (высокодифференцированные опухоли), II степень (умеренно дифференцированные опухоли) и III степень дифференцировки (низкодифференцированные опухоли). Для наиболее часто используемой четырехуровневой характеристики степени дифференцировки опухоли характерны минимальные отличия между опухолями высокой (I и II степени) и низкой (III и IV степени) дифференцировок. С практической точки зрения оправдана бинарная система, при которой все забрюшинные саркомы делят на опухоли низкой и высокой степени дифференцировки. К первым относятся агрессивные опухоли с высокой частотой развития метастазов [1, 12, 16].
Таким образом, для оценки прогноза заболевания, кроме гистологического типа, имеют значение степень дифференцировки и стадия развития опухоли.
Клиническая картина
Из-за анатомических особенностей забрюшинного пространства опухоль головного мозга сколько с ней живут без операции» rel=»dofollow»>опухоль может никак не проявлять себя, пока не достигнет больших размеров. Близлежащие органы не являются препятствием для быстрого роста образования, а рыхлая структура клетчатки забрюшинного пространства позволяет опухолевому процессу беспрепятственно распространяться.
Клинические проявления НЗО характеризуются рядом особенностей. Опухоли не имеют патогномоничных признаков и проявляются обычно симптомами поражения различных органов, нервных стволов и сосудов, вовлекаемых в процесс вторично. Большое разнообразие клинических признаков заболевания объясняется тем, что данные опухоли могут располагаться в забрюшинном пространстве от диафрагмы до малого таза. Именно локализация и размеры новообразования обусловливают те или иные клинические симптомы.
Обнаруживаются опухоли, как правило, случайно. Образования большого размера определяются при осмотре и пальпации больного.
Характер боли тесно связан с местом локализации НЗО. Больные предъявляют жалобы на частые боли в области живота, различные диспепсические расстройства: тошноту, рвоту, задержку стула, вздутие живота. При расположении образования в области таза могут наблюдаться симптомы, характерные для нарушения функции нижних мочевых путей: затруднение, учащение мочеиспускания, императивные (трудно сдерживаемые) позывы к мочеиспусканию, императивное недержание мочи, в поздних стадиях отмечаются гематурия, боли, усиливающиеся при наполнении мочевого пузыря. В свою очередь компрессия магистральных кровеносных и лимфатических сосудов приводит к одышке, отеку и увеличению нижней конечности на поражённой стороне. Более поздние стадии заболевания характеризуются развитием признаков интоксикации: слабость, снижение массы тела, необъяснимый субфебрилитет. Неврологические синдромы, обусловленные компрессией нервных стволов, наблюдаются примерно у 25–30% [2, 7].
Характерной особенностью злокачественных НЗО является высокая склонность к рецидивированию при низком метастатическом потенциале опухоли. Чаще всего метастазируют дизэмбриогенетические опухоли (тератомы, хордомы), реже – гладкомышечные, нейрогенные и ангиогенные саркомы.
Диагностика неорганных забрюшинных опухолей
Диагностика НЗО основывается на данных физикального осмотра, лабораторных и инструментальных методов [7, 9, 13].
Первый этап включает тщательный сбор анамнеза, осмотр и пальпацию. При осмотре больного следует обратить внимание на форму живота, объем нижних конечностей, наличие расширенных вен семенных канатиков с обеих сторон. Все эти симптомы не являются специфичными для НЗО и могут лишь дать основание заподозрить наличие образования, расположенного забрюшинно. НЗО, локализующиеся в малом тазу, характеризуются рядом особенностей, что даtт основание выделять их в группу “тазовых внеорганных забрюшинных опухолей”. Эти опухоли чаще недоступны пальпации через переднюю брюшную стенку и определяются лишь при вагинальном или ректальном исследовании.
Лабораторные методы. Из лабораторных методов исследования наибольшее значение имеет определение уровня человеческого хорионического гонадотропина и α-фетопротеина для идентификации первичной герминогенной опухоли забрюшинного пространства.
Компьютерная томография и магнитно-резонансная томография. КТ и МРТ являются наиболее ценными методами исследования в диагностике забрюшинных опухолей, позволяющими не только уточнить локализацию опухоли, точные размеры новообразования и соотношение его с окружающими тканями, но и выявить метастатические очаги в печени и брюшной полости. Смещение забрюшинно расположенных органов кпереди позволит более точно определить локализацию образования. При этом необходимо исключить его органное происхождение, чему способствует правильная интерпретация ряда признаков. К таким признакам относятся: характер деформации органа, признак фантомного органа (если опухоль головного мозга сколько с ней живут без операции» rel=»dofollow»>опухоль исходит из небольшого по размерам органа, то выявление этого органа не представляется возможным), источник васкуляризации забрюшинного новообразования. Некоторые ретроперитонеальные опухоли обладают рядом КТ- и МРТ-признаков, которые позволяют установить правильный диагноз.
Так, характерной особенностью лимфангиом и ганглионевром является рост между структурами и сосудами забрюшинного пространства без компрессии их просвета, а опухоли симпатической нервной системы растут вдоль симпатической цепочки и имеют продолговатую форму. Выявление источника и интенсивности васкуляризации опухоли – важная задача при КТ- и МРТ-исследовании. К гиперваскуляризованным опухолям относятся гемангиоперицитомы, к умеренно васкуляризованным – злокачественная фиброзная гистиоцитома, лейомиосаркома и, в несколько меньшей степени, другие виды сарком. Липосаркома, лимфома и многие доброкачественные опухоли характеризуются слабой васкуляризацией. Большое значение КТ и МРТ имеют при локализации опухоли в малом тазу для выявления опухолевой инвазии в кости.
Возможность определения характера и плотности содержимого опухоли еще больше суживает диагностический ряд. Липосаркомы и липомы чаще всего встречаются в забрюшинном пространстве. КТ и МРТ позволяют выявить жировую ткань по плотности сигнала, при этом гомогенность и четкие контуры опухоли свидетельствуют о липоме, гетерогенность и отсутствие четких контуров – о липосаркоме. Тератомы также имеют включения, близкие по плотности к жировой ткани, при этом установлению правильного диагноза способствует выявление жидкости и кальцинатов [2, 13]. Нейрогенные опухоли и миксоидные липосаркомы характеризуются наличием миксоидной стромы, богатой кислыми мукополисахаридами, обусловливающей гиперинтенсивные сигналы при МРТ. В опухолях с высокой степенью дифференцировки (например, лейомиосаркомах) обнаруживаются очаги некроза.
Преимуществом КТ по сравнению с МРТ является меньшее количество артефактов, обусловленных движением пациента во время исследования. Неинвазивный характер данных видов исследований, возможность проведения в амбулаторных условиях, небольшое коли- чество противопоказаний являются критериями, позволяющими рассматривать их как основной метод диагностики данной патологии в рутинной практике.
Ультразвуковое исследование. Ультразвуковая диагностика НЗО обладает многими достоинствами, свойственными КТ и МРТ. Преимуществами исследования являются сравнительно небольшая стоимость, доступность и информативность [7, 9, 12].
Биопсия. Биопсия первичных неорганных опухолей, подлежащих оперативному лечению (с учетом данных инструментальных методов обследования), нецелесообразна, поскольку гистологический диагноз не влияет на тактику лечения.
Рентгенологическое исследование. В настоящее время рутинная экскреторная урография используется несколько реже для выявления сдавления или смещения мочеточников, свидетельствующих именно о забрюшинной локализации процесса.
Рентгеноскопия желудочно-кишечного тракта, дополненная ирригоскопией, может выявить смещение, сдавление или прорастание стенки желудка и различных отделов кишечника.
Большую помощь хирургу при выполнении оперативного вмешательства могут оказать данные ангиографии, рентгеноконтрастного исследования сосудов. Анатомической предпосылкой ангиографии являются атипизм ангиоархитектоники и избыточная васкуляризация, которые свойственны многим новообразованиям и отличают их от нормальных тканей. Исследование позволяет выявить как прямые, так и косвенные признаки забрюшинных опухолей.
К прямым ангиографическим признакам относятся:
Илеокаваграфия – контрастное исследование вен, которое имеет большое значение в диагностике НЗО. Тонкая стенка вены и низкое давление в ней обусловливают возникновение деформации контуров сосуда даже при небольших прилежащих образованиях. Этот метод, как и аортография, помогает при решении вопроса о возможности и объеме оперативного лечения опухоли. Зная уровень блокады и степень развития коллатералей, возможно заранее планировать перевязку магистральных вен, в том числе и нижней полой вены [4].
Эндоскопическое исследование. Эндоскопические методы исследования в диагностике забрюшинных опухолей позволяют исключить первичное поражение внутренних органов, а также установить вторичное вовлечение их в процесс за счет прорастания извне. Для диагностики НЗО возможно применение лапароскопии, с помощью которой удается выявить расположение опухоли и диагностировать метастатическое поражение органов брюшной полости.
Лечение
Основным и единственно радикальным методом лечения забрюшинных неорганных опухолей является хирургическое лечение. По данным литературы, хирургическое лечение увеличивает пятилетнюю выживаемость до 50%. Примерно в 60–80% случаев приходится выполнять резекции прилежащих структур, чаще всего почки, толстой и тонкой кишки, поджелудочной железы и мочевого пузыря. Основными принципами вмешательства по поводу забрюшинных опухолей являются удаление опухоли с вовлеченными органами, резекция в пределах здоровых тканей для того, чтобы избежать оставления резидуальной опухоли.
Эффективность хирургического лечения, по данным литературы, колеблется в широких пределах – от 25 до 95%. Даже после радикального хирургического лечения, по данным некоторых авторов, рецидивы продолжают возникать через 5 и 10 лет после выполненной операции, при этом частота локальных рецидивов достигает 50%. Данная цифра может свидетельствовать не только о большой площади поражения опухолевым процессом к моменту выполнения хирургического вмешательства, но и о неэффективности адъювантной лучевой и химиотерапии. Однако, например, забрюшинные липосаркомы характеризуются низкой склонностью к развитию отдаленных метастазов (7%) по сравнению с другими гистологическими подтипами (15-34%), поэтому хирургические вмешательства, выполненные даже с наличием опухолевых клеток по краю резекции, приводят к улучшению выживаемости этих пациентов [10, 11, 15].
Прогноз
В целом забрюшинные неорганные опухоли характеризуются неблагоприятным прогнозом: общая пятилетняя выживаемость, по данным различных авторов, колеблется от 15 до 30% [1, 3].
Клиническое наблюдение 1
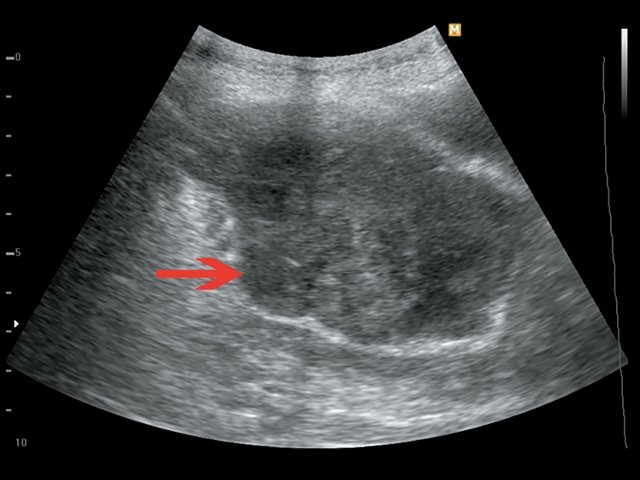
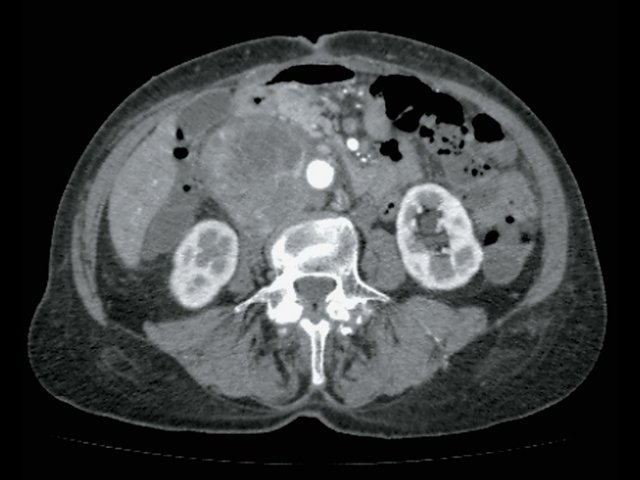
Пациентка Д., 72 года, считает себя больной с апреля 2015 г., когда впервые обратила внимание на стойкую потерю массы тела. При обследовании выявлена неорганная опухоль головного мозга сколько с ней живут без операции» rel=»dofollow»>опухоль забрюшинного пространства. Со слов пациентки оперирована в декабре 2015 г. В настоящее время поступает для утончения диагноза и определения дальнейшей тактики ведения. Пациентке выполнены УЗИ и КТ (рис. 1, 2).
а) B-режим. Забрюшинно справа определяется мягкотканное образование до 8 см в диаметре, с бугристыми контурами, внеорганное, состоящее из множества узлов. Образование оттесняет и сдавливает нижнюю полую вену, распространяясь до правой почечной вены, деформируя нижнюю стенку последней.
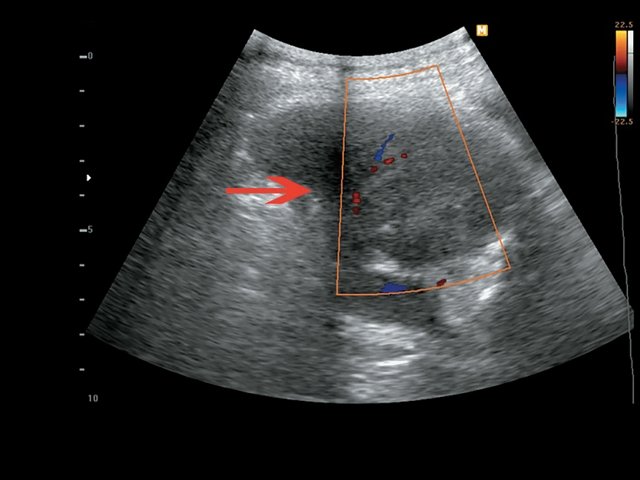
б) Режим ЦДК. Определяется неравномерный кровоток в образовании с преимущественным контрастированием по периферии.
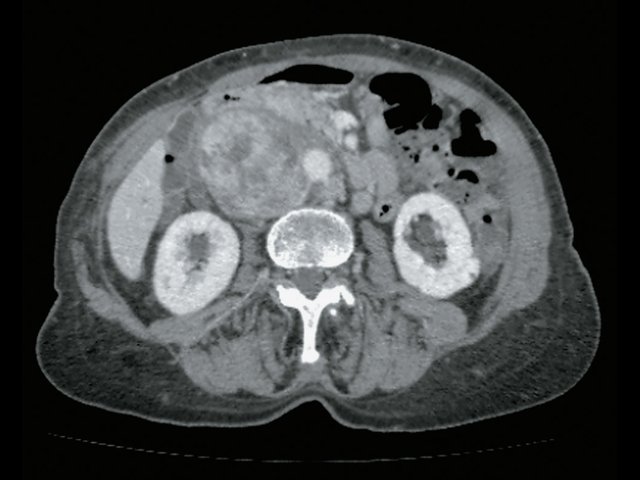
а) Артериальная фаза. Нижняя полая вена на уровне тела позвонка LII (средние отделы) до уровня LIV (верхняя кортикальная пластинка) неравномерно «мешковидно» расширена на протяжении 7,3 см, диаметр на аксиальных срезах 5,1 см, неизмененный диаметр выше расширения 1,4 см, ниже 1,5 см. При введении контрастного вещества в артериальную фазу определяется неоднородная заполняемость просвета за свет наличия заброса из правой почечной вены.
в) Отсроченная фаза. Определяется тугое заполнение полостной системы почек. Признаков сдавления объемным образованием не выявлено.
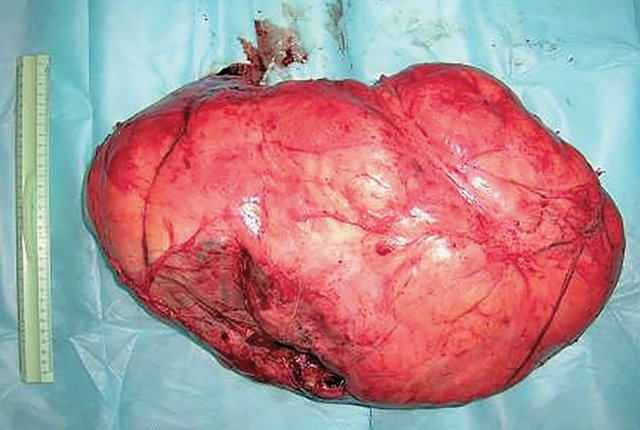
Рис. 3. Макропрепарат. Опухоль желтого цвета 25 х 40 см. Опухоль плотноватой консистенции, на разрезе серовато-жёлтого цвета.
Лечение включало: резекцию объемного образования и правостороннюю нефрэктомию. При гистологическом обследовании опухоль головного мозга сколько с ней живут без операции» rel=»dofollow»>опухоль оказалась лейомиомой с минимальным склерозом. Почка с мелкоочаговым склерозом, гиалинозом сосудов, в канальцах микрокальцинаты (рис. 3).
Клиническое наблюдение 2
Пациент К., 63 года, жалоб не предъявляет. Обследован в ходе проведения диспансеризации. При ультразвуковом исследовании выявлено образование в забрюшинном пространстве (рис. 4, 5).
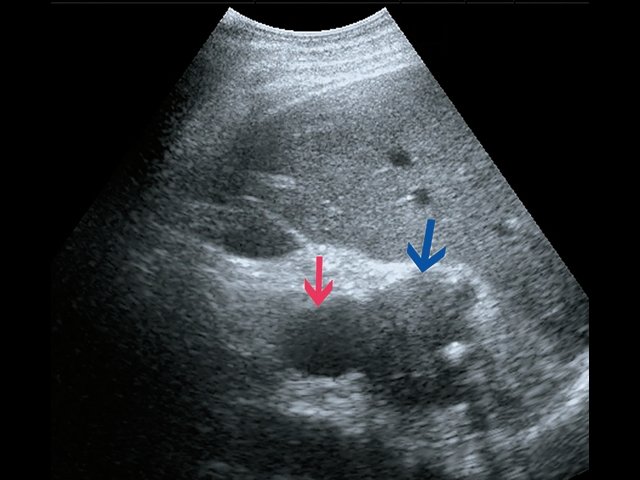
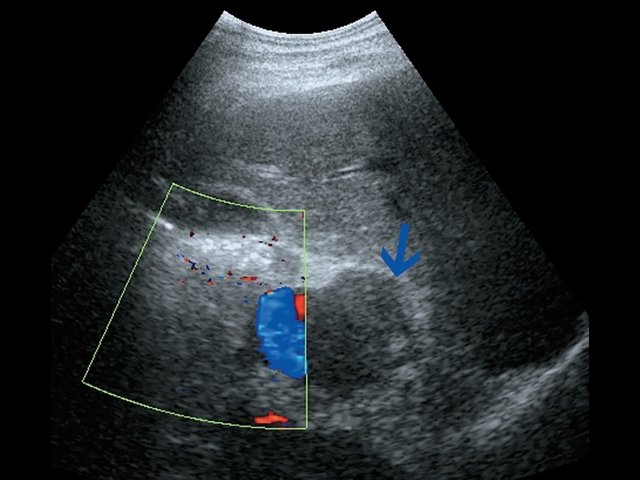
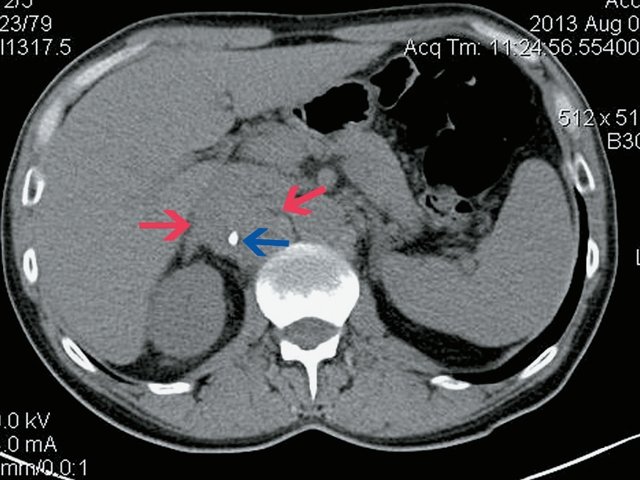
а) В-режим. Визуализируется образование забрюшинно справа, внеорганное, мягкотканное, размером 4,5 см, с кальцинатом (синяя стрелка), оттесняет нижнюю полую вену (красная стрелка).
б) Режим ЦДК. В образовании определяется неравномерный кровоток.
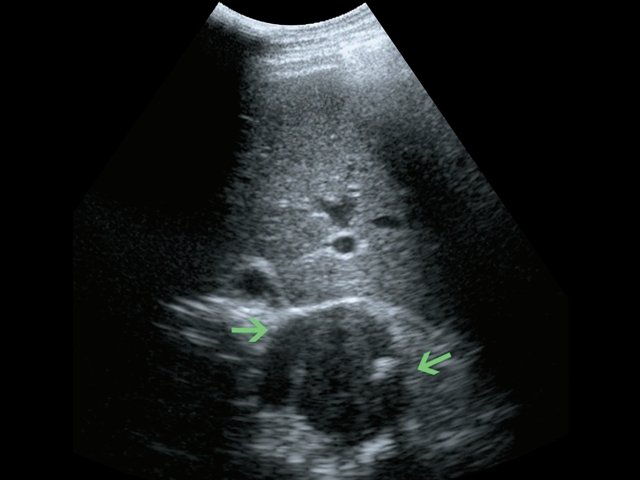
а) В-режим. Забрюшинное образование справа (зеленые стрелки).
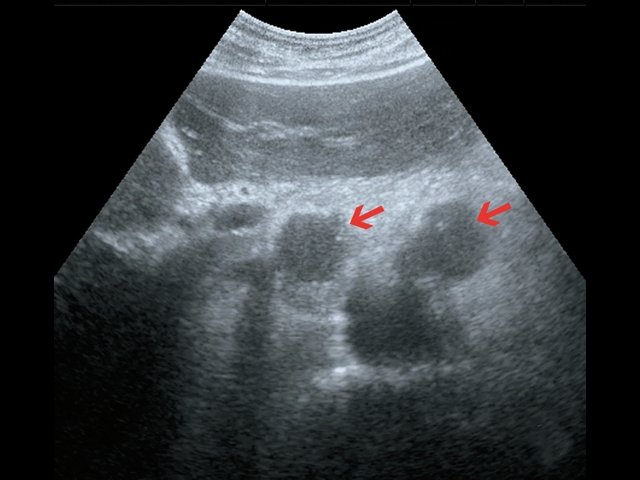
б) В-режим. Забрюшинные лимфатические узлы (красные стрелки).
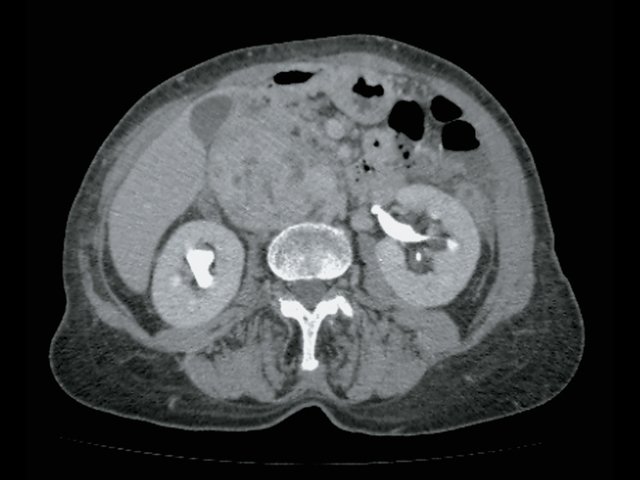
При КТ (рис. 6) установлено: парасагиттально справа, проекционно забрюшинно, преимущественно парааортально, с интимным прилежанием к СI и СVIII печени, оттесняя нижнюю полую вену, определяется неоднородное образование с включением жидкостной плотности, с наличием единичного кальцификата в структуре размер 5,1 х 4,7 х 4,3 см, при внутривенном контрастировании неравномерно накапливает контрастное вещество своим тканевым компонентом. Процесс оттесняет правую почечную вену, последняя без убедительных признаков дефектов наполнения, рядом (в структуре процесса) проходит левая почечная вена. Определяются множественные разнокалиберные парааортальные и паракавальные лимфатические узлы, размерами приблизительно 3,2 х 2,8 см. Заключение: КТ-признаки забрюшинного внеорганного образования справа. Лимфаденопатия.
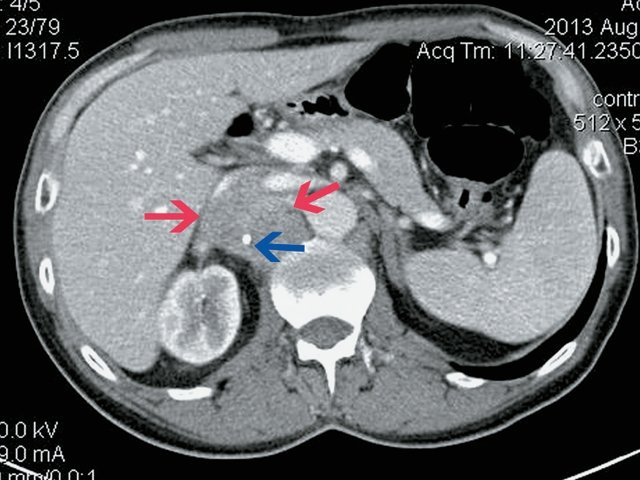
а) Нативная фаза. Забрюшинное образование справа (красные стрелки), кальцинат в нем (синяя стрелка).
б) Артериальная фаза. Образование (отмечено красными стрелками) неравномерно накапливает контраст.
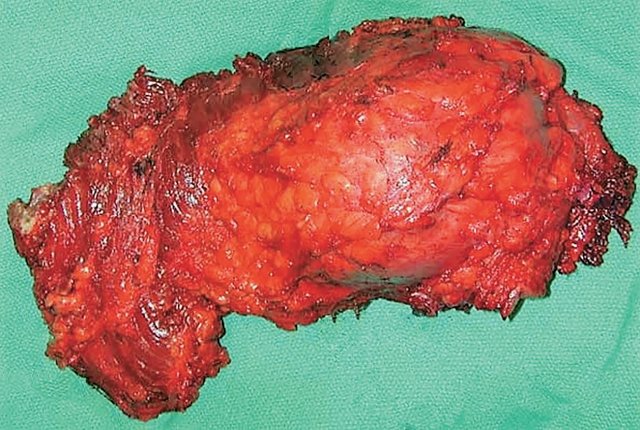
Выполнено оперативное вмешательство в объеме удаления опухоли. Макропрепарат (рис. 7) представлен бугристой рыхлой опухолью желтоватого цвета до 20 см в диаметре. Гистологически выявлена фибролипосаркома.
Рис. 7. Макропрепарат. Опухоль имеет форму узла плотной консистенции, на разрезе желтовато-белого цвета с многочисленными кровоизлияниями.
Клиническое наблюдение 3
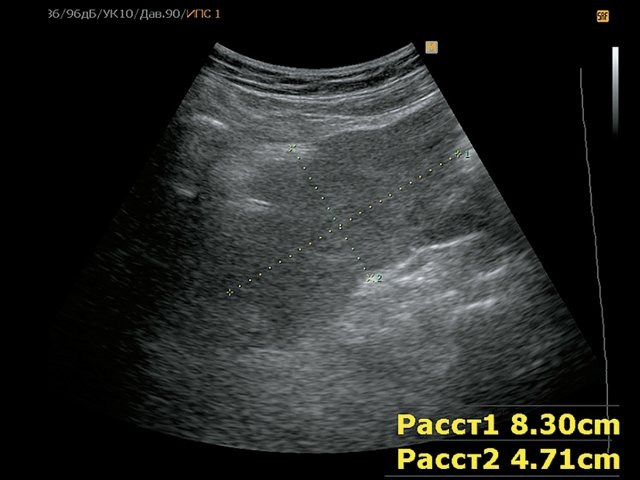
Пациентка П., 43 года, жалоб не предъявляет. Обследована в ходе диспансеризации. При ультразвуковом исследовании малого таза выявлено внеорганное образование (рис. 8). При КТ (рис. 9) в области малого таза справа определяется вне органное объемное образование размером до 8 см, при введении контрастного вещества плотность повышается до +56 ед.H. Проведенная биопсия образования позволила установить диагноз лейомиомы. Учитывая категорический отказ пациентки от оперативного лечения, было решено продолжить динамическое наблюдение.
а) B-режим. Забрюшинно справа определяется внеорганное гипоэхогенное мягкотканное образование неправильной формы, неоднородной эхоструктуры, размером до 8 см.
б) Режим ЦДК. Образование кровоснабжается.