можно ли принимать супракс при гайморите
Каждый, кто хоть раз сталкивался с приемом антибиотиков, знает, что это мощные препараты, которые не назначают просто так. Мы поговорим о препарате Супракс, созданного на основе цефалоспоринов 3 поколения.
Показания
Супракс предназначен для лечения инфекционно-воспалительных процессов, вызванных бактериями, которые чувствительны к цефиксиму. Поэтому перед началом приема необходимо сдать анализы на определение возбудителя инфекции.
Таким образом, Супракс применяют при следующих заболеваниях:
Противопоказания
Антибиотик имеет ряд противопоказаний, среди них:
Побочные эффекты
Во время терапевтического лечения Супракс может вызвать следующие побочные эффекты:
Обычно данные побочные реакции не проявляются достаточно ярко и слабо выражены. Поэтому в большинстве случаев не требуют прекращения лечения.
Как принимать Супракс
Согласно инструкции по применению, Супракс принимают 1 раз в день внутрь вне зависимости от приема пищи.
Как правильно пить Супракс
Капсулы для приема внутрь
Суспензия для приема внутрь
Чтобы правильно приготовить суспензию, встряхните гранулы во флаконе, постепенно влейте в него 40 мл прохладной воды, каждый раз тщательно взбалтывая до образования однородной суспензии. Если приготовление во флаконе невозможно, то стоит использовать стеклянную либо эмалированную посуду. Для полного растворения гранул, стоит дать постоять получившемуся раствору около пяти минут. Суспензию Супракс можно не хранить в холодильнике.
Продолжительность курса терапии зависит от диагноза, тяжести течения заболевания, наличия осложнений и особенностей организма пациента. Ее определяет лечащий врач. В среднем лечение длится 7-10 дней.
Стоит отметить, что при продолжительном приеме Супракса у пациента может возникнуть хроническая диарея и последующее развитие тяжелого колита.
Также, на фоне приема лекарственного средства могут наблюдаться головокружения или приступы сильной головной боли. Лучше воздерживаться от управления автомобилем, сложной техникой, требующей немедленного реагирования или концентрации.
Супракс во время беременности и ГВ
Прием Супракса во время беременности назначается только при наличии угрозы жизни матери. Причем это возможно только во втором и третьем триместрах. В первом триместре прием Супракса может вызвать аномалии или врожденные уродства у плода.
Супракс при беременности
В период лактации Супракс противопоказан. Если препарат все-таки назначен, необходимо перевести ребенка на искусственное вскармливание.
Аналоги Супракса
Знаете, чем именно Супракс лучше аналогов? Он применяется для лечения агрессивных возбудителей, и достаточно эффективно. И все это амбулаторно! Также препарат может применяться постепенно, то есть у врача есть возможность назначить ступенчатую терапию. Это необходимо при довольно серьезных случаях. Лечение начинают с парентеральных форм цефалоспоринов 3 поколения, а через 2-3 дня, когда состояние пациента улучшилось, переходят на пероральный прием Супракса.
Аналогичным терапевтическим эффектом с капсулами Супракс обладают следующие препараты:
Синонимами (препаратам, имеющими в составе то же действующее вещество) являются:
Помните, что заменять один препарат другим может только лечащий врач, который учитывает не только тяжесть состояния пациента, характер течения болезни, но и противопоказания и возможные побочные эффекты.
Супракс/Панцеф
В основе данных антибиотиков одно и то же активное вещество. Если ориентироваться на отзывы пациентов, то при приеме Панцефа организм реже проявляет негативные реакции в виде побочных эффектов.
Супракс/Сумамед
Сумамед в своей основе содержит азитромицин, который обладает более широким антимикробным действием. Сумамед назначают детям, он вызывает меньше побочных эффектов и продолжительность курса меньше.
Супракс/Амоксиклав
В отличие от Амоксиклава Супракс лучше переносится и реже вызывает дисбактериоз и другие расстройства ЖКТ.
Дополнительная информация о препарате
Итак, цефалоспорины – антибиотики, которые характеризуются широким спектром воздействия, они отличаются высокой бактерицидностью и невосприимчивостью к бета-лактамазам (ферментам бактерий, которые разрушают антибиотик, в результате чего его действие становится неэффективным). В общем, в каком-то смысле, цефалоспорины эффективнее пенициллинов. И вот в основе Супракса как раз цефалоспорины третьего поколения. И это первый такой антибиотик, который можно принимать внутрь. В основе Супракса – цефиксим. Цефиксим влияет на клеточную стенку патогена, угнетая ее образование.
Супракс угнетает жизнедеятельность стрептококков, гемофильной, кишечной палочки, протей, сальмонеллы, цитробактера и гонококков. Однако Супракс бессилен перед синегнойной палочкой, большинством стафилококков, энтеробактеров и листерий. Что касается приема препарата, то еда никак не влияет на его биодоступность. Да, удлиняет период достижения максимального содержания в крови и только. Супракс еще хорош тем, что принимать его нужно один раз за день. Это связано с временем полувыведения препарата из организма. Он выводится долго. С мочой выходит около 50% лекарства. И это здорово, потому что это эффективно помогает при лечении инфекций мочевыводящих путей. Однако с диуретиками его лучше не принимать, так как вывод лекарства замедляется. Вообще Супракс отлично проникает к месту инфекции. Основными очагами инфекции, с которыми взаимодействует Супракс, являются полость среднего уха, придаточные пазухи носа, миндалины, легкие, желчные пути. Если ориентироваться на отзывы пациентов о приеме Супракса, то они отмечают незначительное угнетение миклофлоры кишечника. Вы можете найти Супракс в двух лекарственных формах, которые ориентированы на разные возрастные группы: капсулы по 400 мг для взрослых пациентов и гранулы для приготовления суспензии с клубничным вкусом 100 мг/5 мл – 60 мл для детей.
Эффективность перорального цефалоспорина III поколения при ЛОР-патологии у детей
Рассмотрены принципы назначения антибактериальных препаратов при бактериальных инфекциях ЛОР-органов. Показана эффективность применения цефиксима в амбулаторной педиатрической практике в качестве стартового препарата.
Principles of antibacterial preparations prescription in bacterial infections of ENT-organs were considered. The efficiency of cifixim inoutpatient pediatric practice as a start preparation was shown.
Острые воспалительные заболевания ЛОР-органов лидируют по обращаемости за медицинской помощью и назначению антимикробных (в том числе и антибактериальных препаратов). Ведущее место в их структуре занимают риносинусит и острый средний отит (особенно у детей первых лет жизни) [1–4]. Из года в год ведущими бактериальными агентами для этих заболеваний у детей признаются Streptococcus pneumoniae и Haemophilus influenzae, несколько реже встречаются Sreptococcus pyogenes, Moraxella catarrhalis [2–9]. Последние исследования подтверждают ведущую роль Streptococcus pneumoniae и при острых [2, 3, 9, 11], и при рецидивирующих средних отитах [9–11].
Основные принципы назначения антибактериальных препаратов при данной патологии представлены в табл. 1.
Кроме того, в выборе стартового препарата для антибактериальной терапии при острых воспалительных заболеваниях ЛОР-органов следует учитывать региональные данные о спектре и чувствительности бактериальных возбудителей к антибактериальным препаратам и путь введения препарата (на этапе амбулаторного лечения основу терапии должны составлять пероральные препараты с высокой биодоступностью). В противном случае, при нерациональном подходе к подбору антибиотика, велик риск формирования резистентности микроорганизмов и хронизации течения воспалительных процессов ЛОР-органов.
В настоящее время основными препаратами в терапии гнойно-воспалительных заболеваний ЛОР-органов с пероральным путем введения является группа β-лактамов. Наиболее распространены среди них: аминопенициллины и цефалоспорины. При аллергии на β-лактамные антибиотики к применению ранее рекомендовались макролиды (азитромицин, кларитромицин) [3, 5, 11, 12], однако, согласно последней версии рекомендаций Американской академии пародонтологов (American Academy of Periodontology, AAP)/Американской академии семейных врачей (American Academy of Family Physications, AAFP) (2013) [9], пациентам с острым средним отитом (ОСО) рекомендуется при наличии в анамнезе IgE-опосредованных аллергических реакций на пенициллины назначать цефалоспорины, достоинствами которых является высокая избирательность действия на прокариотическую клетку и связанная с этим безопасность применения у новорожденных и беременных, меньший аллергенный потенциал по сравнению с пенициллинами и быстрое бактерицидное действие. Особенно хорошо зарекомендовали себя пероральные цефалоспорины III поколения как препараты с удобным режимом дозирования (1–2 раза в сутки), а также высоким уровнем антибактериальной активности по сравнению с цефалоспоринами предыдущих поколений в отношении пенициллинорезистентных пневмококков, Haemophilus influenzae и Moraxella catarrhalis. Их достоинствами являются особенности фармакокинетики, позволяющие сохранять высокие концентрации действующего вещества в слизистой оболочке околоносовых пазух. Механизм бактерицидного действия цефалоспоринов связан с нарушением процесса образования клеточной стенки бактерий. Мишень их действия, как у всех β-лактамных антибиотиков, — пенициллиносвязывающие белки, которые выполняют важную роль на завершающем этапе синтеза пептидогликана — биополимера, являющегося основным и обязательным компонентом клеточной стенки бактерий. Поэтому почти все микроорганизмы, имеющие клеточную стенку, чувствительны к действию цефалоспоринов [14]. До недавнего времени цефалоспорины были представлены в основом парентеральными формами и получили широкое применение на этапе стационарного лечения. В настоящее время появились препараты этой группы и для перорального применения, одним из которых является цефиксим (Супракс).
Цефиксим разрешен к применению у детей с 6 месяцев, характеризуется широким спектром действия и высокой активностью в отношении основных бактериальных возбудителей ЛОР-патологии (в том числе штаммов Haemophilus influenzae, устойчивых к аминопенициллинам и цефалоспоринам I поколения), а также обладает активностью в отношении бактерий семейства Enterobacteriaceae.
В последнее время все чаще упоминаются возможные взаимодействия между различными патогенами. Так, например, Moraxella catarrhalis способствует усилению адгезии пиогенного стрептококка (β-гемолитического стрептококка группы А (БГСА)) к клеткам эпителия дыхательных путей (ко-адгезия) [15, 16]. Цефиксим элиминирует M. сatarrhalis, тем самым обеспечивая высокую степень эрадикации пиогенного стрептококка (количество (КОЕ) S. pyogenus, адгезированных к эпителию носоглотки, снижается в 10 раз) [15], что позволяет рекомендовать его не только при РС/ОСО, но и при тонзиллофарингитах (ТФ), так и сам цефиксим обладает высокой активностью непосредственно против БГСА. Напомним, что основным показанием к назначению антибактериального препарата при ТФ является выделение БГСА [3, 5]. Этот возбудитель выявляется и как ведущий бактериальный агент при остром среднем гнойном отите у детей, занимая второе место (13,7%) после Streptococcus pneumoniae (47,7%) (О. В. Бугайчук, Е. Ю. Радциг, Е. П. Селькова 2014).
Цефиксим (Супракс) не подавляет рост условно-патогенной микрофлоры (например, альфа-гемолитического стрептококка), в норме присутствующей на слизистой верхних дыхательных путей, предотвращая колонизацию/инфекцию носоглотки истинными патогенами (S. pneumoniae, H. influenzae, S. aureus, пиогенный стрептококк).
Эффективность препарата оценивалась неоднократно [14, 18–22], приведем результаты одного из последних ретроспективных анализов данных по эффективности и безопасности цефиксима у детей с различной ЛОР-патологией, ставившего задачей оценку эффективности и безопасности препарата Супракс (цефиксим) в рутинной педиатрической практике. Критерии включения и исключения представлены в табл. 2.
Под наблюдением находился 61 пациент с различной инфекционной патологией ЛОР-органов, среди них (рис. 1):
Всем пациентам было показано назначение антибактериальной терапии, в качестве стартового препарата был выбран цефиксим (Cупракс), назначенный в соответствии с инструкцией: детям в возрасте от 6 месяцев до 12 лет назначали суспензию в дозе 8 мг/кг/сутки (по цефиксиму: рекомендуемая продолжительность приема препарата — 7 дней (РС/ОСО) — 10 дней (ТФ)).
Оценка применения препарата Супракс (цефиксим) в группе пациентов с различными формами острого среднего отита (34 (55,7%) пациента)
Из 34 пациентов у 11 (32,4%) были различные стадии гнойного среднего отита (перфоративная у 7 пациентов и доперфоративная — у 4). У 23 (67,7%) пациентов диагностирован катаральный средний отит. Возраст пациентов варьировал от 1 до 12 лет, средний возраст составил 5,6 года, преобладали мальчики (22 пациента (64,7%)). Длительность симптоматики до обращения к врачу составила 1–4 дня, в среднем первый визит к врачу состоялся на 2,5 день от появления первых симптомов. Характер течения заболевания был оценен как острый и тяжесть течения заболевания как среднетяжелая у всех 34 пациентов. Выздоровление фиксировалось на 5–8 день от начала лечения. Средняя продолжительность приема препарата цефиксим (Супракс) составила 6,7 дней.
Не было эффекта от проводимого лечения, включающего прием препарата цефиксим (Супракс), у 3 (8,82%) пациентов с неперфоративной формой среднего гнойного отита. Эти пациенты были госпитализированы в стационар, где им был проведен парацентез.
Оценка применения препарата Супракс (цефиксим) в группе пациентов с различными формами острого риносинусита (21 (34,4%) пациент)
В данной группе была выявлена следующая патология:
Возраст пациентов варьировал от 3 до 11 лет, средний возраст — 5,6 года. Среди пациентов было 15 (71,4%) мальчиков и 6 (28,6%) девочек. Длительность симптоматики до обращения к врачу колебалась от 1 до 13 дней, в среднем первый визит к врачу состоялся на 7,5 день от появления первых симптомов. Характер течения заболевания был оценен как острый у 21 (100%) пациента; тяжесть течения заболевания как легкая у 7 (33,3%) и среднетяжелая у 14 (66,7%) пациентов. Выздоровление фиксировалось на 5–9 день от начала лечения. Средняя продолжительность приема препарата цефиксим (Супракс) составила 6,9 дня.
Оценка применения препарата Супракс (цефиксим) в группе пациентов с различными формами острого тонзиллита/тонзиллофарингита (6 пациентов (9,8%))
У 3 (50,0%) пациентов был острый тонзиллит, у 1 (16,7%) — острый тонзиллофарингит и у 2 (33,3%) пациентов — обострение хронического тонзиллита. В данной группе было 4 (66,7%) мальчика и 2 (33,3%) девочки в возрасте от 5 до 12 лет, средний возраст составил — 9,1 года. Длительность симптоматики до обращения к врачу колебалась от 1 до 2 дней, в среднем первый визит к врачу состоялся на 1,8 дня от появления первых симптомов. Характер течения заболевания был оценен как острый у 4 (66,7%) и обострение хронического у 2 (33,3%) пациентов. Выздоровление фиксировалось на 7–10 день от начала лечения. Средняя продолжительность приема препарата цефиксим (Супракс) составила 8,4 дня.
Данные о клинической эффективности и переносимости препарата у пациентов всех групп представлены на рис. 2.
Ни у одного пациента (0%) на фоне приема препарата не было отмечено нежелательных лекарственных реакций.
Выводы
Вышеизложенное позволяет рекомендовать препарат цефиксим (Супракс) для использования в амбулаторной педиатрической практике в качестве стартового препарата при бактериальных инфекциях ЛОР-органов.
Литература
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Положительный опыт комплексного консервативного лечения острого и хронического гайморита в стадии обострения
Д. м. н., проф. А.Ю. Овчинников, к. м. н. М.А. Панякина
Первый МГМУ им. И.М. Сеченова, кафедра болезней уха, носа и горла, Москва
Проблема воспалительных заболеваний околоносовых пазух на сегодняшний день крайне актуальна и имеет большое социальное значение. Помимо того, что риносинусит является крайне распространенным заболеванием, он наносит весьма ощутимый финансовый урон обществу, так как наибольшее число больных — люди в возрасте от 18 до 55 лет, то есть наиболее активная и трудоспособная часть населения. В последнее время отмечается ежегодный прирост заболеваемости на 1,5-2%. В силу определенных анатомических особенностей чаще других поражаются верхнечелюстные пазухи.
Рост воспалительных заболеваний околоносовых пазух происходит в первую очередь из-за серьезных экологических сдвигов, в частности, возросшей загрязненности и загазованности воздушной среды, увеличения числа респираторных вирусных инфекций, количества ингалируемых аллергенов, снижения резервных возможностей верхних дыхательных путей, возросшей резистентности флоры в результате нерационального применения антибиотиков.
Физиология
Приступая к обсуждению этиологии и патогенеза синусита, следует определиться с терминологией и классификацией. Чаще всего бактериальный синусит развивается у здорового человека на фоне респираторной вирусной инфекции, и лечение заболевания проводится в амбулаторных условиях. Эту основную по численности группу синуситов называют внебольничными. Помимо нее существуют госпитальные, одонтогенные синуситы, а также синуситы, развившиеся у больных с иммунодеффицитными состояниями. Возбудители и патогенез этих форм принципиально различаются.
Переходя к рассмотрению микробного пейзажа синусита, следует подчеркнуть, что вирусное инфицирование является лишь первой фазой заболевания, и оно «прокладывает путь» бактериальной инфекции. В условиях нормального функционирования механизма мукоциллиарного транспорта бактерии не имеют возможности для достаточно длительного контакта с клетками эпителия полости носа. При поражении слизистой оболочки вирусом продлевается время контакта патогенных бактерий с клетками и становится возможным вторичное бактериальное инфицирование.
Ранее существовало представление о стерильности околоносовых пазух. Однако это вряд ли возможно, так как согласно законам нормальной физиологии околоносовые пазухи имеют постоянный контакт с другими отделами верхних дыхательных путей, где постоянно вегетирует самая разнообразная микрофлора. Возбудителями инфекционного синусита могут быть как патогенные, так и условно-патогенные микроорганизмы. Последние являются естественными обитателями организма человека и вызывают заболевания при снижении местного и общего иммунитета. Именно представители условно-патогенной микрофлоры являются наиболее значимыми возбудителями бактериального синусита, подтверждая положение, что при любом синусите в той или иной степени страдает иммунитет.
Среди возбудителей синусита наиболее значимыми в настоящее время являются S.pneumoniae, H.influenzae, реже встречается Moraxella catarrhalis.
Нарушение нормальных анатомических взаимоотношений в полости носа изменяет аэродинамику, способствуя попаданию неочищенного воздуха в околоносовые пазухи, повышая тем самым риск развития воспаления.
Среди других возбудителей выделяют Moraxella catarrhalis (примерно в 4% случаев у взрослых и 12% у детей) и стрептококки других групп.
В условиях нормального функционирования механизма мукоциллиарного транспорта бактерии не имеют возможности для достаточно длительного контакта с клетками эпителия полости носа. При поражении слизистой оболочки вирусом продлевается время контакта патогенных бактерий с клетками и становится возможным вторичное бактериальное инфицирование.
Препараты терапии
Антибиотики для местного воздействия. Многочисленные исследования показали, что препараты для местного воздействия особенно эффективны в лечении синусита в тех случаях, когда хорошо проходимы естественные соустья пазух. Кроме того, существует целый ряд работ, показывающих целесообразность использования местных препаратов у больных после различных операций в полости носа и околоносовых пазухах, когда особенности течения послеоперационного периода диктуют необходимость проведения именно местного лечения. Преимуществами местной терапии в данном случае являются: непосредственное воздействие на послеоперационную область, возможность создания оптимальной концентрации препарата в очаге, отсутствие системного действия за счет крайне низкой их системной абсорбции.
Системная антибиотикотерапия является основным направлением в лечении инфекционных синуситов за рубежом. Наличие широкого выбора эффективных антибактериальных средств, исчерпывающей информации о чувствительности и природной резистентности к ним микроорганизмов, с определенной частотой ассоциированных с тем или иным заболеванием, а также отсутствие надежных методов ускоренной бактериологической диагностики превращают эмпирическую антибактериальную терапию в наиболее рациональную стратегию этиотропной терапии в период возникновения острых гнойных или обострения хронических синуситов на начальном этапе их лечения.
Огромный арсенал современных антибиотиков, безусловно, расширяет возможности клинициста. Успешной реализации указанных задач способствует хорошая ориентированность в спектре действия, в фармакокинетике, микробиологическом влиянии препарата, а также информированность о его доказанной эффективности и безопасности. Большинство ошибок при назначении антибиотика в амбулаторной практике связано именно с неправильным выбором препарата. Главным критерием при этом по-прежнему является возможность воздействия на основных возбудителей воспаления. Приоритетом для выбора того или иного препарата служит не широкий, а оптимальный спектр антибактериальной активности, то есть тот, что охватывает наиболее значимые по статистическим данным в настоящее время и наиболее вероятные именно для данного больного возбудители. Другая проблема при назначении антибиотиков заключается в отсутствии учета уровня приобретенной резистентности возбудителей в популяции. Бесконтрольное и зачастую необоснованное применение ряда антибактериальных средств привело к росту региональной резистентности, что нашло отражение в исследованиях по данной проблеме. Сведения об активности различных групп антибиотиков в отношении «главного» возбудителя острого синусита Streptococcus pneumoniae показывают следующее: имеется тенденция к снижению чувствительности к бета-лактамам. Устойчивость к пенициллину в России не превышает 2%, но штаммы с умеренной чувствительностью составляют 10-20%. Бета-лактамы сохраняют полную клиническую эффективность в отношении пенициллин-резистентных пневмококков, но определяется снижение эффективности цефалоспоринов 1-2-го поколения.
Спектр значимых возбудителей и характер резистентности в отношении антибактериальных препаратов в настоящее время таковы, что для терапии гнойных синуситов на современном этапе используют β-лактамы, фторхинолоны и макролиды.
Достаточно высокой эффективностью при лечении синуситов обладают цефалоспорины, которые на протяжении 40 лет занимают ведущие позиции среди антибиотиков. Достоинствами, объясняющими такое долголетие, являются:
Пероральные цефалоспорины 3-й генерации. Супракс (цефиксим) хорошо зарекомендовал себя как препарат с удобным режимом дозирования (1 раз в сутки), а также высоким уровнем антибактериальной активности по сравнению с цефалоспоринами предыдущих поколений, в отношении пенициллин-резистентных пневмококков, а также β-лактам-устойчивых гемофиллов и моракселл. Достоинством препарата Супракс (цефиксим) является оптимальная фармакокинетика в ЛОР-органах, позволяющая сохранять высокие концентрации действующего вещества в слизистой оболочке околоносовых пазух.
На фоне применения препарата восстанавливается секреция IgA, улучшается мукоцилиарный транспорт, происходит регенерация структур слизистой оболочки. Действие препарата распространяется на слизистую оболочку всех отделов дыхательного тракта. Одновременное назначение карбоцистеина и антибиотиков потенцирует лечебную эффективность последних при воспалительных процессах в области как верхнего, так и нижнего отдела дыхательного тракта. Кроме того, Карбоцистеин взаимно повышает эффективность глюкокортикостероидной терапии, усиливает бронхолитический эффект теофиллина. Активность Карбоцистеина ослабляют противокашлевые и атропиноподобные средства.
Материалы и методы
Для подтверждения тезиса о возможности консервативной терапии синуситов нами проведено обследование и лечение 65 больных, страдающих острым или хроническим гайморитом в стадии обострения, диагноз которого устанавливался на основании жалоб, анамнестических данных, результатов оториноларингологического осмотра, лабораторного и инструментального обследования.
Следует отметить, что данная группа была сформирована из больных, отказавшихся от проведения им пункционного метода лечения. Для лечения 39 больных нами была использована следующая схема лечения:
Распределение больных по полу было приблизительно одинаковым. Среди них было 39 женщин (60%) и 26 мужчин (40%) в возрасте от 18 до 63 лет (39 ± 10,82 лет). Следует отметить, что 67% больных находились в активном трудоспособном возрасте (20-50 лет).
На неэффективность предшествующего пункционного лечения указывали 18 (28,1%) больных. У 60 (92,3%) больных после проведенного микробиологического исследования была выявлена патогенная микрофлора (табл. 1).
Таблица 1.
Число штаммов микроорганизмов, выделенных до начала лечения
| Возбудитель | Число штаммов | % |
| Streptococcus pneumoniae | 14 | 17 |
| Haemophilus influenzae | 12 | 14,6 |
| Streptococcus pyogenes | 11 | 13,4 |
| Streptococcus viridans | 8 | 9,8 |
| Staphylococcus epidermidis | 8 | 9,8 |
| Candida albicans | 7 | 8,5 |
| Staphylococcus aureus | 6 | 7 |
| Moraxella catarrhalis | 6 | 7 |
| Mycoplasma pneumoniae | 5 | 6 |
| Chlamydia pneumoniae | 3 | 4,6 |
| Всего | 82 | 100 |
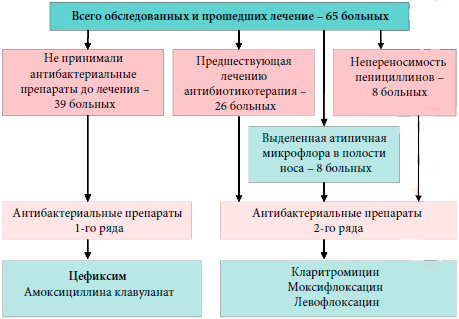
У 7 из 65 больных на третьи сутки после начала лечения отсутствовала положительная динамика субъективных и объективных симптомов гайморита. Этим больным дополнительно назначен курс пункционного лечения до получения результатов микробиологического исследования ввиду опасности развития внутричерепных осложнений. 4 из них после получения данных бактериологического исследования была произведена коррекция схемы лечения в соответствии с антибиотикограммой. У 2 больных был выделен золотистый стафилококк, резистентный к большинству антибиотиков. Назначен ципрофлоксацин по 500 мг 2 раза в сутки в течение 5 дней. У 2 больных выявлен также резистентный к большинству антибиотиков эпидермальный стафилококк. Антибиотиком 2-го ряда стал левофлоксацин по 500 мг 1 раз в сутки в течение 5 дней. У 3 оставшихся больных возбудители не были идентифицированы, назначен антибактериальный препарат 2-го ряда (Моксифлоксацин в дозировке 500 мг 1 раз в сутки в течение 5 дней). У остальных больных, схема лечения не претерпела каких либо изменений (рис. 1).
Рис. 1. Схема антибактериальной терапии больных
В результате проведенного лечения у всех больных отмечена нормализация картины периферической крови, что выражалось в статистически значимом (р 7 ).
Заключение оториноларинголога: Острый двусторонний гнойный гайморит. Аллергический рино-синусит.
Заключение пульмонолога: скрытая бронхоконстрикция.
Больная принимала Супракс (цефиксим) по 400 мг 1 раз в день в течение 10 дней, Флюдитек (карбоцестеин) по 750 мг (15 мл сиропа) 3 раза в сутки в течение 10 дней. Ксилометазолина гидрохлорид 0,1%-ный по 2-3 капли в каждую ноздрю 3 раза в день на протяжении 7 дней.
Через 2 дня после начала лечения головная боль прекратилась, периоды затрудненного носового дыхания сократились, появились обильные выделения из носа слизисто-гнойного характера. Через 5 дней насморк не прекратился, однако выделения приобрели слизистый характер, значительно уменьшился отек и гиперемия слизистой оболочки, восстановилось обоняние.
За последующие 5 дней слизистая оболочка полости носа приобрела равномерную розовую окраску, полностью исчез ее отек и стали обозримы средние носовые ходы. Сохранялись периодические слизистые выделения из носа.
При повторном бактериологическом исследовании роста микрофлоры выявлено не было. Сахариновое время для правой и левой половин носа уменьшилось соответственно до 17 и 15 мин.
Спустя 30 дней больная жалоб не предъявляла, а риноскопическая картина полностью нормализовалась.
Однако по-прежнему многие практические врачи крайне скептически относятся к попыткам беспункционного лечения гайморита, называя в качестве главного аргумента неизбежную хронизацию процесса при использовании только системной антибактериальной терапии. Ошибочная постановка знака равенства между пункцией и антибактериальной терапией нередко приводит к нежелательным последствиям. В случае консервативного, неинвазивного лечения должна быть найдена альтернатива пункции как дренирующему мероприятию для эвакуации патологического секрета из пазухи, начиная с медикаментозных средств и заканчивая щадящими инструментальными пособиями. А индивидуальный подход к каждому конкретному больному с учетом частой сопутствующей патологии со стороны нижних дыхательных путей позволит в значительной мере оптимизировать результаты лечения и избежать частых обострений и рецидивов со стороны как верхнего, так и нижнего отдела дыхательной системы.

.gif)
.gif)
.gif)