можно ли при тиреотоксикозе делать операцию
Тиреотоксикоз
Общая информация и формы тиреотоксикоза
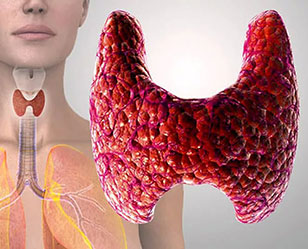
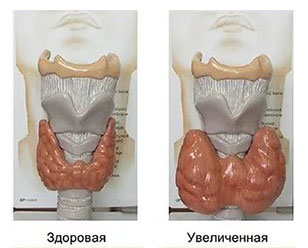
В результате воздействия различных факторов или при течении некоторых заболеваний щитовидной железы в организме образуется переизбыток ее гормонов. Такое состояние называется тиреотоксикоз (гипертериоз) – интоксикация организма избыточным количеством гормонов.
К основным причинам развития тиреотоксикоза относят заболевания щитовидной железы (многоузловой и диффузный токсический зоб, токсическая аденома, различные формы тиреоидитов), а также передозировку гормональных препаратов при лечении гипотериоза.
Поскольку патологиями щитовидной железы чаще страдают женщины в возрасте 20–50 лет, то и тиреотоксикоз развивается именно у этой категории пациентов.
Формы тиреотоксикоза
В зависимости от гормонального уровня и степени тяжести тиреотоксикоза выделяют три формы патологического состояния:
Симптомы тиреотоксикоза
Проявления тиреотоксикоза зависят от формы патологического состояния. В самом начале пациентов беспокоят периодические головные боли, бессонница, тревожность, раздражительность. На фоне более существенного изменения гормонального фона нарушается работа сердечно-сосудистой и нервной систем: появляется тахикардия, одышка, повышается артериальное давление. Для тяжелой формы характерно значительное снижение веса, нарушения в половой сфере, увеличение объема шеи, развитие офтальмопатии (слезотечение, двоение в глазах и т.д.), экзофтальма (выпячивание и увеличение глазных яблок).
При появлении первых симптомов тиреотоксикоза обязательно обратитесь к эндокринологу, ведь вовремя обнаруженная патология гораздо легче поддается лечению.
Диагностика тиреотоксикоза
Для того чтобы точно определить характер заболевания и его стадию, необходимо пройти тщательное обследование. В нашем Центре есть все, что нужно для быстрой и качественной диагностики тиреотоксикоза.
На первой консультации эндокринолог беседует с пациентом, собирает детальный анамнез, проводит пальпацию области шеи. Для определения уровня гормонов щитовидной железы наши пациенты сдают анализы крови на ТТГ, Т3 и Т4 свободные. Следующий этап диагностики – проведение УЗИ щитовидной железы для выяснения объема органа и характера кровотока в нем.
Полученные данные позволяют врачу составить полное представление о течении тиреотоксикоза, его форме и разработать план лечения.
Оперативное лечение тиреотоксикоза
Если у вас диагностирована тяжелая форма тиреотоксикоза или курсы консервативной терапии оказались неэффективными, эндокринолог предложит хирургическое лечение.
В нашем Центре для устранения симптомов тиреотоксикоза и лечения сопутствующих заболеваний щитовидной железы проводят тиреоидэктомию. Операция направлена на полное удаление щитовидной железы вместе с капсулой. Хирургическое вмешательство проводится с использованием открытого доступа – врач выполняет разрез длиной 30–40 мм на передней поверхности шеи. Затем хирург выделяет возвратно-гортанные нервы и удаляет щитовидную железу. Послеоперационную рану ушивают саморассасывающимся шовным материалом.
При тиреоидэктомии мы используем гармонический скальпель Harmonic Focus – это позволяет избежать сильных кровотечений и травмирования голосовых нервов, снизить болевой синдром в послеоперационном периоде, ускорить процесс восстановления.
Записаться на консультацию к эндокринному хирургу Центра можно по телефону +7 (495) 292-59-87.
Тиреотоксикоз: операция или радиойодтерапия
Когда нужно рассматривать вопрос о радикальном лечении тиреотоксикоза?
Референсные значения антител к рецепторам ТТГ:
Каковы симптомы этого состояния и его причины?
Какой метод лечения выбрать: операция или радиойодтерапия
Как уже отмечалось выше, если пациент в течение долгого времени (более 2-х лет) принимает (или принимал) тиреостатический препарат, а длительная ремиссия так и не наступила, – это уже веский повод для принятия решения о применении радикального метода лечения. Если такое решение, наконец, принято, то неизбежно возникает вопрос: «Какой метод лечения выбрать?«
На сегодняшний день радикальных методов лечения тиреотоксикоза два: хирургическое вмешательство и радиойодтерапия (РЙТ).
Сразу оговоримся, что задача обоих методов – добиться полного угасания функции щитовидной железы с последующим переходом на пожизненную заместительную терапию гормоном левотироксином (Л-тироксин или Эутирокс).
На что стоит обратить внимание при выборе хирургического лечения?
Щитовидная железа – богато кровоснабжаемый орган и достаточно сильно кровоточит при операции. Здесь находится много нейро-сосудистых пучков, которые можно травмировать.
Изначально маленький объем ЩЖ (без узловых образований) – также НЕ лучшая ситуация для операции.
Учитывая вышесказанное, если пациент все же принимает решение о хирургическом удалении щитовидной железы при диффузно-токсическом зобе – лучшим выбором объема операции будет тотальная тиреоидэктомия, или предельно субтотальная тиреоидэктомия, то есть удаление полностью всей ткани щитовидной железы, ради минимизации риска рецидива в будущем.
Хирургическое вмешательство будет правильным в случае узлового зоба, то есть наличия узла (тем более, нескольких узлов) в щитовидной железе, которые при сцинтиграфии окажутся «холодными» (не накапливающие радиофармпрепарат).
Естественно, прежде чем, выбирать тот или иной метод лечения, необходимо убедиться в доброкачественной природе данных узловых образований, что достигается путем выполнения тонкоигольной аспирационной биопсии (ТАБ). Золотой стандарт – проведение ТАБ под контролем ультразвука, из нескольких мест, а также соответствие описания биопсии международному протоколу Tirads.
Когда делать операцию на щитовидной железе?
Щитовидная железа отвечает за секрецию гормона щитовидной железы, который жизненно важен для метаболизма. Этот гормон регулирует клеточный метаболизм. В некотором смысле именно это гормон определяет, насколько быстро функционируют клетки.
Изначально можно разделить все заболевания щитовидной железы на две группы: функциональные и структурные. Обе группы содержат большое разнообразие болезней.
Функциональные расстройства, первая группа, вызваны нарушением уровня гормонов. Пациенты этой группы могут испытывать чрезмерную или недостаточную функцию щитовидной железы, что влияет на уровень секреции гормона, что в свою очередь вызывают определенные проблемы в организме.
Вторая группа связана с болезнями, вызванными структурными изменениями в этих железах. Пациенты, у которых присутствуют узелки, доброкачественные и злокачественные (раковые) опухоли в щитовидной железе, относятся к последней группе.
Когда делать операцию на щитовидной железе?
Оперативное вмешательство является вариантом лечения для заболеваний щитовидной железы. Однако выполнение операции у пациента в нужное время требует знаний и навыков, в то время, как успех операции с минимальными побочными эффектами требует особого таланта и опыта. Главный хирург Медицинского Центра Анадолу, профессор, доктор медицинских наук Метин Чакмакчы (Metin Çakmakçı) отвечает на наши вопросы по оперативному лечению щитовидной железы и на частый вопрос пациентов «Когда делать операцию на щитовидной железе?».
Каких пациентов с щитовидной железой можно оперировать?
В основном мы рассматриваем вариант хирургического лечения при заболеваниях щитовидной железы для трех основных групп: первая группа пациентов это те, у которых диагностирован рак щитовидной железы с помощью биопсии тонкой иглой или те, чьи результаты биопсии патолог считает сомнительными в отношении рака.
Ко второй группе пациентов относятся те, у которых выявлены симптомы сжатия или косметические проблемы в связи с увеличением узелков. Мы могли бы рекомендовать оперативное решение проблемы, если мы заметим изменения в размерах узелков у пациентов, наблюдающихся по поводу подозрения на рак.
Третья группа состоит из больных с гипертиреозом — состоянии, при котором щитовидная железа перепроизводит этот гормон. Мы рекомендуем оперативное лечение больных с гипертиреозом, независимо от медикаментозного лечения или лечения радиоактивным йодом, а также для случаев рецидивирующего гипертиреоза. Хирургическое лечение также применяется у пациентов с побочными эффектами на медикаментозное лечение или лечение радиоактивным йодом или у тех, кто не может получать такое лечение из-за проблем, таких как беременность.
Что определяет метод лечения у больных с гипертиреозом?
Мы можем лечить гипертиреоз тремя различными методами – медикаментозное лечение, лечение радиоактивным йодом или оперативным методом. Лекарства, применяемые для подавления секреции гормона щитовидной железы, снижают скорость функционирования этой железы. Радиоактивный йод уменьшает объем тканей, вырабатывающих гормон, разрушая клеточную структуру щитовидной железы. Хирургическое лечение, с другой стороны, включает в себя частичное или полное удаление щитовидной железы, очищая организм от избытка тканей, вырабатывающих гормон щитовидной железы. Мы принимаем решение после тщательной оценки пользы того или иного вида лечения для пациента. При принятии решений о выборе лечения мы также рассматриваем такие факторы, как возраст, пол, предыдущее лечение, сопутствующие заболевания и результаты скрининговых тестов таких, как УЗИ и сцинтиграфия.
Какой метод лечения предпочтителен для пациентов, планирующих иметь детей?
Вариант лечения радиоактивным йодом не рассматривается, если пациент все еще находится в периоде активной фертильности или планирует иметь детей. Мы используем медикаментозное или хирургическое лечение для таких пациентов.
Каковы шансы рецидива при медикаментозном лечении?
Изначально мы отдаем предпочтение медикаментозному лечению у пациентов с гипертиреозом. Однако самая большая проблема при медикаментозном лечении — это рецидив после курса лечения. Рецидивы встречаются у многих пациентов в течение одного года после окончания курса применения лекарств. Только 20 процентов пациентов остаются здоровыми в течение 5 лет после окончания медикаментозного лечения. Более того, некоторые пациенты не могут использовать какие-либо лекарства из-за значительных побочных эффектов. Связанные с применением лекарств побочные эффекты, означают, что у многих пациентов остается один выбор лечения – операция.
В чем заключается операция на щитовидной железе?
Основной принцип оперативного лечения гипертиреоза заключается в сокращении объема вырабатывающей гормон щитовидной железы. Благодаря этому методу у большинства пациентов остается нормально функционирующая щитовидная железа после операции. Однако небольшое число пациентов все же сталкивается с рецидивом гипертиреоза, и это может вызвать проблемы в лечении. Кроме этого, существует риск развития гипотиреоза, если оставшаяся ткань щитовидной железы не способна вырабатывать достаточное количество гормона, необходимого организму. Тем не менее, шансы такого осложнения достаточно небольшие и контроль уровня гормонов при помощи лекарственных препаратов очень прост.
Опыт в сочетании с достижениями в области технологий, включая новые источники энергии, открыл путь для более безопасных и эффективных гипертиреоидных операций. Такое развитие событий привело к увеличению популярности операций по тиреоидэктомии. Этот метод подразумевает полное удаление щитовидной железы, устраняя шансы рецидива.
Как часто встречается узловой зоб?
Исследования показывают, что число людей с узловым зобом составляет около 10%. Секционные патологоанатомические исследования указывают на более высокую частоту.
Все ли виды узелкового зоба свидетельствуют о раке?
Хотя шансы встретить узелки достаточно высоки, процент рака щитовидной железы является относительно низким. Другими словами, люди не должны думать, что все узелки означают рак. На самом деле мы склонны считать, что большинство узелков являются доброкачественными.
Является ли операция единственным решением для любого вида узелкового зоба?
Все узелки следует воспринимать всерьез и тщательно исследовать, хотя операция требуется не для любого узелка, обнаруженного в щитовидной железе. Исследуя узелки пациента, мы должны принять во внимание жалобы, медицинский анамнез, результаты обследований и скрининга. В принципе, для узелков меньше 1 см, не имеющих радиологического риска, достаточно периодического наблюдения. Мы рекомендуем провести аспирационную биопсию тонкой иглой для узелков размером более 1 см, которые попадают в группу риска. В последнее время, биопсия тонкой иглой приобрела популярность наряду с наработками в цитологии (дисциплина, изучающая клетки) и интервенционной радиологией. Благодаря биопсии тонкой иглой, заведомо сомнительные или раковые (по заключению патологов) узелки немедленно удаляются хирургическим путем. Сегодня рак щитовидной железы остается одним из нескольких типов рака, эффективно поддающихся лечению с помощью хирургических методов.
Рассматривается ли вариант операции для доброкачественных узлов?
Хирургическое лечение существует даже для доброкачественных узлов. Большие или растущие узелки могут вызвать жалобы такие, как трудности при глотании и боль. Их размер может вызвать косметические проблемы из-за их видимости. Хирургическое лечение может применяться у таких пациентов. Мы предпочитаем удалять щитовидную железу в полном объеме в случаях рака щитовидной железы и гипертиреоза. Оперативное лечение носит ограниченный характер у больных с доброкачественными случаями. В таких случаях мы удаляем часть, содержащую наибольший узелок. Мы стремимся оставить максимум здоровой ткани, чтобы организм продолжал вырабатывать достаточное количество гормонов щитовидной железы. При необходимости мы выполняем экспресс — патологические исследования на одном из этапов операции и, соответственно, определяем дальнейший ход операции.
Лечение тиреотоксикоза
Тиреотоксикоз обусловлен избыточной секрецией тиреоидных гормонов щитовидной железой и встречается при многих клинических состояниях. Причинами развития тиреотоксикоза могут быть: диффузный токсический зоб (ДТЗ, болезнь Грейвса, болезнь Базедова); аутоим
Тиреотоксикоз обусловлен избыточной секрецией тиреоидных гормонов щитовидной железой и встречается при многих клинических состояниях. Причинами развития тиреотоксикоза могут быть: диффузный токсический зоб (ДТЗ, болезнь Грейвса, болезнь Базедова); аутоиммунный тиреоидит в фазе тиреотоксикоза; функциональная автономия (токсическая аденома, многоузловой токсический зоб); йод-индуцированный тиреотоксикоз; резистентность к тиреоидным гормонам; ТТГ-продуцирующая аденома; гестационный транзиторный тиреотоксикоз; метастазы рака, продуцирующие тиреоидные гормоны; Struma ovarii; ятрогенный тиреотоксикоз; тиреотоксическая стадия подострого тиреоидита (де Кервена).
При наличии у пациента клинических симптомов тиреотоксикоза, прежде чем приступать к лечению, очень важно точно установить причину его развития, поскольку от этого будет зависеть адекватность выбранного метода терапии.
Гормональными маркерами гиперфункции, равно как и других заболеваний щитовидной железы, являются тиреотропный гормон (ТТГ) и свободный тироксин (св.Т4). В тех случаях когда при исследовании ТТГ оказывается сниженным, а св. Т4 в пределах нормы, проводится определение свободного трийодтиронина (св.Т3) с целью диагностики Т3-тиреотоксикоза (рис.1). На следующем этапе диагностики необходимо установить причину тиреотоксикоза. В медицинской практике нам наиболее часто приходится наблюдать пациентов с аутоиммунными заболеваниями щитовидной железы — ДТЗ и аутоиммунный тиреоидит. ДТЗ обусловлен выработкой тиреостимулирующих иммуноглобулинов (ТСИ), которые связываются с рецептором ТТГ на мембранах тиреоцитов и через активацию циклического аденозинмонофосфата постоянно стимулируют повышенную секрецию тиреоидных гормонов. Исследование антител к рецептору ТТГ (АТ-рТТГ) не только позволяет подтвердить диагноз ДТЗ, но и дифференцировать его с аутоиммунным тиреоидитом (АИТ).
Показания для определения АТ-рТТГ в клинической практике
В практике врача уже стало традиционным определение антител к тиреоглобулину (АТ-ТГ) и к тиреопероксидазе (АТ-ТПО). Выявление этих антител позволяет легко решить проблему диагностики либо в пользу АИТ, либо — ДТЗ. На этот факт следует обратить особое внимание, поскольку АТ-ТГ и АТ-ТПО могут обнаруживаться в достаточно большом количестве как у больных АИТ, так и у пациентов с ДТЗ. Более того, по данным исследований, эти антитела могут выявляться у части здоровых людей и у пациентов с заболеваниями щитовидной железы неаутоиммунного генеза. И наконец, не во всех случаях при АИТ и ДТЗ антитела можно обнаружить. Следовательно, проводить диагностику на основании только одного признака и тем более решать вопрос о целесообразности назначения лечения не представляется возможным. В диагностике АИТ помимо определения АТ-ТПО большое значение имеет ультразвуковое исследование щитовидной железы (УЗИ).
Неравномерное диффузное снижение эхогенности ткани служит надежным признаком АИТ, но тем не менее не позволяет дифференцировать его с ДТЗ, для которого характерным являются те же изменения по УЗИ. Таким образом, диагноз АИТ должен основываться на комплексе клинических и лабораторно-диагностических признаков. УЗИ щитовидной железы позволяет определить объем ткани, наличие узлового образования, что очень важно, поскольку у части пациентов эти показатели могут повлиять на выбор стратегии лечения.
Сцинтиграфия щитовидной железы у больных тиреотоксикозом проводится при подозрении на наличие функциональной автономии (токсическая аденома, многоузловой токсический зоб), загрудинный зоб, нефункциональные участки более 1–1,5 см.
Лечение ДТЗ (болезни Грейвса)
В настоящее время существуют три метода лечения ДТЗ: консервативный; радиоактивным йодом ( 131 I); хирургический.
Каждый из этих методов имеет свои показания, а также противопоказания и должен назначаться каждому пациенту индивидуально.
1. Консервативное лечение
Консервативную терапию назначают больным с небольшим диффузным увеличением щитовидной железы (по объему — 35–40 мл) без симптомов сдавления.
У пациентов с большим объемом щитовидной железы и/или узловыми образованиями по размерам более 1,0-1,5 см, а также с тяжелыми осложнениями тиреотоксикоза консервативную терапию используют в качестве медикаментозной подготовки к хирургическому лечению. При планировании радиойодтерапии пациентам также предварительно назначают консервативное лечение.
На фоне тиреостатической терапии эутиреоидное состояние наступает уже через 3–5 нед от начала лечения. В течение последующих 12–24 мес поддерживающей эутиреоз терапии примерно у 20–40% пациентов развивается ремиссия заболевания.
К сожалению, у части пациентов примерно через год вновь «расцветает» клиника тиреотоксикоза. Таким больным нецелесообразно назначать повторные длительные курсы консервативной терапии. Вероятнее всего, ТСИ продолжают вырабатываться в большом количестве и стимулировать щитовидную железу к избыточной продукции тиреоидных гормонов. В подобных случаях проводят курс медикаментозной подготовки, а затем, в зависимости от размеров и морфологических изменений ткани щитовидной железы, назначают либо терапию 131 I, либо оперативное лечение. Прогноз ремиссии или возможного рецидива тиреотоксикоза после проведения курса тиреостатической терапии можно определить по уровню АТ-рТТГ. Исследование антител проводится перед полной отменой препаратов. Риск рецидива тиреотоксикоза у пациентов возрастает при повышенном уровне АТ-рТТГ, чаще рецидивы наблюдаются в течение первого года после окончания лечения.
Для лечения ДТЗ на протяжении многих лет используются препараты из группы тионамидов: тиамазол (тирозол, мерказолил, тиамазол-филофарм, метизол, метимазол) и пропилтиоурацил (пропицил). C появлением дозировки тирозола 10 мг количество принимаемых таблеток можно уменьшить в 2 раза, что создает дополнительное удобство для пациентов. Механизм тиреостатического действия заключается в подавлении синтеза тиреоидных гормонов на стадиях органификации и комплексирования. Пропилтиоурацил частично подавляет превращение Т4 в Т3 за счет ингибирования 5’-монодейодиназы. Лечение тиреостатическими препаратами начинают с относительно высоких доз: 30–40 мг тиамазола или его аналогов 2–3 приема в день в течение дня или 300 мг пропилтиоурацила — 3–4 приема в день. После достижения эутиреоза дозу постепенно снижают до поддерживающей: тиамазол до 5–10 мг в день, пропилтиоурацил до 50–100 мг 1–2 приема в день (рис). Достижение эутиреоидного состояния оценивается по исчезновению клинических симптомов тиреотоксикоза и уровню св. Т4. Определять уровень ТТГ нецелесообразно, поскольку на протяжении нескольких месяцев он может оставаться подавленным. Дополнительно в лечении ДТЗ используют β-адреноблокаторы, которые подавляют тканевое превращение Т4 в Т3. Пропранолол назначают по 60–120 мг/сут 3–4 приема в день, атенолол — 50–100 мг/сут, конкор — 5–10 мг/сут однократно. В клинической практике существует два варианта назначения тиреостатических препаратов: в виде монотерапии или в комбинации с левотироксином (эутирокс, L-тироксин, тиро-4). В последнем варианте пациенту по достижению эутиреоидного состояния (оценивается по уровню Т4) подключают левотироксин в дозе 25–50 мкг. Исследования показывают, что на фоне комбинированной поддерживающей терапии в течение 18–24 мес достигается более стойкая блокада секреции тиреоидных гормонов.
При лечении тиреостатическими препаратами у пациентов могут развиться побочные эффекты в виде аллергических реакций (зуд, крапивница и др.). Одним из наиболее серьезных осложнений является агранулоцитарная реакция. Поэтому пациентам рекомендуется проводить общий анализ крови в первые 7–10 дней после начала лечения, а в дальнейшем — 1 раз в мес. К другим крайне редким тяжелым побочным эффектам относится тромбоцитопения, острый некроз печени.
2. Терапия радиоактивным йодом
Во многих странах мира радиойодтерапия — наиболее часто рекомендуемый метод лечения как ДТЗ, так и других форм токсического зоба, в частности функциональной автономии. Необходимо отметить, что 131 I назначают больным в любом возрасте (дети, пациенты молодого, среднего и пожилого возраста). Единственным противопоказанием для радиойодтерапии является беременность и грудное вскармливание. Спорным остается вопрос о лечении 131 I пациентов ДТЗ в сочетании с эндокринной офтальмопатией. Согласно результатам рандомизированного исследования, у части больных ДТЗ терапия 131 I способствовала прогрессированию эндокринной офтальмопатии. У пациентов, получающих радиойодтерапию, ремиссия тиреотоксикоза наступает в 90–95% случаев. Рецидив заболевания возможен у 3–5% больных, что требует проведения повторного курса радиойодтерапии. Радиоактивный йод принимают перорально в виде натриевой соли 131 I в растворе или капсулах: 131 I быстро поступает в щитовидную железу, вызывая деструкцию тиреоцитов посредством β-излучения. Чаще всего возникает вопрос о выборе больших или малых доз радиойода. Как известно, большие дозы неминуемо приводят к развитию гипотиреоза, использование же малых доз сопряжено с возможностью сохранения клиники тиреотоксикоза. Многолетние исследования за пациентами показали, что однократная доза радиоактивного йода, рассчитанная на полное разрушение щитовидной железы, излечивает тиреотоксикоз у 90% больных. Применение малых доз сохраняет эутиреоидное состояние в течение 10 лет после радиойодтерапии лишь у 25–30% больных. К сожалению, из-за дефицита 131 I нам довольно редко приходится пользоваться этим методом в лечении больных с тиреотоксикозом.
3. Хирургическое лечение
Показаниями для оперативного лечения больных с тиреотоксикозом служат большие размеры зоба, непереносимость тиреостатиков, рецидив тиреотоксикоза после проведенной консервативной терапии, загрудинно расположенный зоб. При наличии показаний возможно хирургическое лечение в I и II триместрах беременности, которое заключается в проведении субтотальной резекции щитовидной железы с оставлением минимального количества (объема) ткани. Однако нередко возникает проблема с определением этого минимального объема ткани. Если оставить меньше 4 г тиреоидной ткани, то неминуемо разовьется гипотиреоз, и тогда возникает необходимость в назначении заместительной терапии левотироксином. В тех случаях когда ткани оставляют больше 4–6 г, довольно часто после операции сохраняются клинические симптомы тиреотоксикоза, возможно, не столь выраженные. Это состояние иногда называют «ложный рецидив». Большой объем оставшейся после операции тиреоидной ткани создает условия для продолжения избыточной секреции тиреоидных гормонов под стимулирующим влиянием ТСИ. Подобная хирургическая тактика, с одной стороны, повышает риск развития осложнений, в частности мерцательной аритмии, а с другой — нередко заканчивается повторной операцией. Согласно вышеизложенному, если пациенту показано оперативное лечение, то целесообразно проводить максимально субтотальную резекцию щитовидной железы, оставляя не более 3 мл ткани. Безусловно, это требует высокой квалификации хирурга, поскольку, как известно, оперативное лечение сопряжено с развитием ряда осложнений, таких как парез возвратного нерва, удаление паращитовидных желез. Операцию следует проводить на фоне эутиреоидного состояния, достигнутого с помощью тиреостатической терапии. При непереносимости тиреостатиков используют β-адреноблокаторы или йод (насыщенный раствор калия йодида или раствор Люголя — 8–10 капель в день в течение 10–12 дней до операции).
Лечение аутоиммунного тиреоидита в фазе тиреотоксикоза
Довольно часто АИТ верифицируется как ДТЗ, поскольку клинические симптомы идентичны, а АТ-ТГ и АТ-ТПО выявляются почти с одинаковой частотой при одном и другом заболевании. Определение АТ-рТТГ в настоящее время пока еще доступно не во всех городах России. Лечение тиреотоксической стадии АИТ проводится чаще консервативно (при отсутствии аргументированных показаний в пользу оперативного вмешательства), при этом в терапии используют β-адреноблокаторы или же их комбинацию с тиреостатическими препаратами. Следует заметить, что тиреотоксикоз на фоне АИТ имеет некоторые особенности: быстрый эффект при приеме тиреостатических препаратов с развитием медикаментозного гипотиреоза; в ряде случаев волнообразное течение заболевания со сменой состояний тиреотоксикоза и эутиреоза.
Лечение функциональной автономии (токсическая аденома, узловой и многоузловой токсический зоб)
Пациентам с тиреотоксической формой функциональной автономии назначают тиреостатические препараты (тирозол, мерказолил, тиамазол-филофарм, метизол, метимазол, пропицил) с целью подготовки к оперативному лечению. В нашей стране из-за дефицита лечебного 131 I больных с функциональной автономией оперируют, хотя во многих странах мира основным методом лечения этих состояний является радиойодтерапия. Автономные участки тиреоидной ткани хорошо захватывают радиойод, который разрушает только эти участки ткани щитовидной железы. Большинство пациентов в дальнейшем переходят в эутиреоидное состояние. Радиойодтерапия предпочтительна особенно у больных пожилого возраста. К операции прибегают при большом объеме автономной ткани щитовидной железы (более 3 см в диаметре).
ТТГ-индуцированный тиреотоксикоз (резистентность к тиреоидным гормонам и ТТГ-продуцирующая аденома гипофиза)
Синдром генерализованной резистентности встречается довольно редко (в литературе описаны около 600 случаев). В связи с тем что у человека чувствительность органов и тканей к тиреоидным гормонам неодинакова, у одного и того же пациента могут развиваться как эутиреоидное, гипотиреоидное, так и гипертиреоидное состояния. Резистентность периферических тканей способствует компенсаторному повышению секреции тиреоидных гормонов, сохраняя, таким образом, эутиреоидное состояние. Если гипофиз оказывается более резистентным по сравнению с периферическими тканями, то развиваются клинические симптомы тиреотоксикоза, которые очень трудно поддаются медикаментозному лечению. Исследования показали, что лечебным эффектом обладает 3,5,3’-трийодтироуксусная кислота. Особенностью этого синдрома является отсутствие подавления ТТГ даже при использовании сверхбольших доз L-Т4, поэтому снижение ТТГ с помощью тиреоидных гормонов абсолютно неэффективно. При обнаружении ТТГ-продуцирующей аденомы гипофиза показано оперативное лечение.
Подострый тиреоидит (де Кервена) развивается спустя некоторое время (4–6 нед) после перенесенной вирусной инфекции. В течении подострого тиреоидита различают тиреотоксическую стадию, которая сменяется гипотиреоидной стадией, а затем в большинстве случаев тиреоидная функция полностью восстанавливается. Назначение β-адреноблокаторов (пропранолол, атенолол, бетаметазон) снимает симптомы тиреотоксикоза, применение препаратов из группы тионамидов не требуется. Пациентам рекомендуется лечение глюкокортикоидами. Преднизолон назначают по 30–40 мг ежедневно в течение 2–3 нед с последующим постепенным снижением дозы на 5 мг в нед. Возможен и другой вариант назначения глюкокортикоидов — 30–40 мг ежедневно в течение 10–12 дней с последующим переводом на прием через день в этой же дозе на протяжении 6–8 нед. Прогноз заболевания, как правило, благоприятный.
Нередко в кардиологической практике пациентам с нарушениями ритма назначают ритмиодарон, амиодарон, кордарон, седакорон. Следует отметить, что эти лекарственные средства способны изменять уровень тиреоидных гормонов у исходно эутиреоидных пациентов. Более чем у 50% больных, принимающих постоянно амиодарон, повышен уровень Т4 (в среднем на 44% по сравнению с базальным уровнем за счет нарушения превращения Т4 в Т3). Следовательно, изолированное повышение Т4 при терапии амиодароном нельзя интерпретировать как диагностический признак тиреотоксикоза. Тем не менее примерно у 5–20% пациентов эти препараты вызывают гипертиреоз, который обычно сопровождается дальнейшим повышением уровня Т4 на фоне значительного снижения уровня ТТГ с развитием симптомов тиреотоксикоза. Наиболее информативный контроль функции щитовидной железы при длительной терапии амиодароном или кордароном оказывается при условии определения ТТГ. Пациентам с «амиодароновым» тиреотоксикозом к терапии подключают β-адреноблокаторы.
Тиреотоксикоз при беременности повышает риск выкидыша, преждевременных родов и рождения плода с малой массой тела. У женщины при этом чаще развивается токсикоз, а в ряде случаев сердечная недостаточность. Одной из наиболее распространенных причин тиреотоксикоза у беременных женщин является ДТЗ. Оптимальным вариантом при его развитии на фоне беременности является ее прерывание. Однако если женщина настаивает на сохранении беременности, то обычно назначают пропилтиоурацил в дозе 25–50 мг в два приема, поскольку при приеме мерказолила у плода иногда наблюдается дефект кожи на голове. Кроме того, пропилтиоурацил имеет более короткий период полужизни и вызывает меньше осложнений по сравнению с тионамидами. В случае использования тионамидов следует назначать минимально эффективные дозы (5–10 мг тирозола в сут) с ежемесячным контролем свободных фракций тиреоидных гормонов. Большие дозы препаратов могут привести к развитию зоба и гипотиреоза у плода. Слабое стимулирующее действие на щитовидную железу оказывает хорионический гонадотропин (ХГ), концентрация в крови которого на ранних сроках беременности возрастает.
У незначительного числа беременных женщин именно ХГ способствует развитию транзиторного тиреотоксикоза. Это состояние не требует лечения. Относительно тяжелый тиреотоксикоз может наблюдаться при пузырном заносе или хориокарциноме.
В этих случаях пузырный занос удаляют или принимают меры, направленные на хориокарциному.
Послеродовый тиреоидит развивается спустя 1–3 мес после родов. Симптомы тиреотоксикоза носят транзиторный характер, сменяясь в дальнейшем гипотиреозом со спонтанной ремиссией через 6–8 мес. Транзиторная стадия тиреотоксикоза не требует лечения, а в гипотиреоидной стадии назначают левотироксин в дозе, которая способствует нормализации ТТГ.
Л. В. Кондратьева, кандидат медицинских наук, доцент
РМАПО, Москва